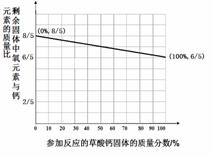
当温度达到800℃以上,该反应生成的固体开始高温分解。如图是在400℃~500℃“剩余固体中氧元素与钙元素的质量比”随着“参加反应的草酸钙固体的质量分数”变化的一次函数关系图像。
⑴根据图像,剩余固体中氧元素与钙元素的质量比为6/5时,剩余固体的组成 ;当参加反应的草酸钙固体的质量分数达到60%时,剩余固体中氧元素与钙元素的质量比 。(用最简分数表示)
⑵当温度超过800℃以后,氧元素与钙元素的质量比最小值为 (用最简分数表示)。
当剩余固体中氧元素与钙元素的质量比为4/5 时,则参加反应的固体的质量分数为 。
如图,A是一种金属氧化物,其相对分子质量为40,B、D、G、H均为单质,
且E、H为空气中的常见气体,J为蓝色难溶性碱,其中化学反应①和③的反应物、生成物以及反应条件已经全部给出。
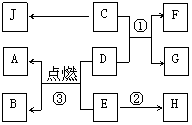 |
⑴写出A的化学式 J的化学式 。
⑵写出下列化学方程式:反应①
反应②
Na2O2是一种淡黄色固体,能与H2O、CO2、HCl等物质反应。某兴趣小组结合化学课学习的内容,探究Na2O2能否和氢气反应。
(已知无水CuSO4是白色粉末,遇水变成蓝色,碱石灰是氢氧化钠固体与生石灰的混合物)
①按图组装仪器,(图中夹持仪器省略)
②检查气密性(气密性良好),装入药品Na2O2
③打开K1、K2,产生的氢气流经装有Na2O2 的硬质玻璃管,一段时间后没有任何现象;
④检验氢气的纯度后,开始加热,观察到硬质玻璃管内Na2O2开始熔化,淡黄色的粉末渐渐变成了白色固体,干燥管内的硫酸铜未变蓝色;
⑤反应后撤去酒精灯,待硬质玻璃管冷却后关闭K1 。

请回答下列问题:
⑴B装置的作用 (填字母)。
A.吸收氢气中混有的氯化氢气体 B.吸收氢气携带的水蒸气
C.吸收装置A、B中空气中的二氧化碳
⑵步骤③目的是 。
⑶步骤⑤关闭K1后,将看到A装置中的现象
| |
⑷通过现象可知Na2O2能和氢气反应。请推测它们反应的生成物 (填字母)。
A. NaOH B. Na2CO3、H2O C. NaOH、H2O D. NaOH、O2
已知硝酸钾、硝酸钠、碳酸锂不同温度时的溶解度(见下表)
|
物质 | 0℃ | 20℃ | 40℃ | 60℃ | 80℃ |
| 硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 |
| 硝酸钠 | 69.5 | 82.3 | 100.6 | 121.8 | 148.4 |
| 碳酸锂 | 1.55 | 1.33 | 1.18 | 1.00 | 0.82 |
在20℃时,向三支试管中分别加入10mL的水,然后分别加入硝酸钾、硝酸钠、碳酸锂三种物质各4g,充分振荡后静置,观察到的现象如图。
⑴请根据上表溶解度,推测试管1中加入的物质 。
⑵分别给上述的三支试管加热至40℃(水分不蒸发), 观察到试
管 (填序号)中的固体渐渐消失。试管3中的溶液溶质质量分数
与加热前相比 (填“增大”或“减小”或“不变”)。
⑶在40℃时,若要使试管3中的溶液形成饱和溶液,则应向试管 3中至少再加入 g
该溶质。(保留1位小数)

在实验室里进行如图所示的实验。当看到红色变成无色时停止实验。
⑴此时能判断烧杯中的溶液一定是中性吗? 。(填“能”或“不能”)
⑵为了验证烧杯中稀盐酸是否过量,又继续进行了如下实验
| 操作 | 现象 | 结论 |
| 取少量烧杯中的液体于试管中,滴加适量的碳酸钠溶液 。 | 无气泡产生,液体变成
|
|
⑶老师又向该试管中加入了足量的氯化钙溶液,观察到的现象是 。
请写出该反应的化学方程式 。当大家把这支试管中的一系列现象与试管中的物质组成进行分析,发现⑵、⑶实验观察到的现象都与 (填一种微粒的符号)的存在有关。
⑷若氢氧化钠溶液与稀盐酸恰好完全反应,要证明有新物质生成可进行 操作。
 |
书写化学方程式错误的类型包括:A.物质化学式书写错误 B.未配平 C.未标注反应条件或条件不对 D.遗漏“↑”或“↓”。下列化学方程式错误的类型是(填序号).
| 序号 | 化学方程式 | 错误类型 |
| ① |
| |
| ② |
| |
| ③ | 2CO+Fe2O3 |
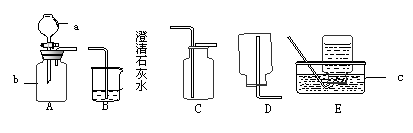 实验室用下列装置可进行一系列的实验。
实验室用下列装置可进行一系列的实验。