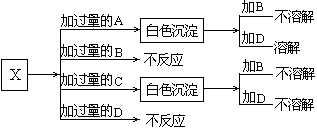
含钠元素的某白色固体X易溶于水,取少量溶液进行如下实验:
 |
据以上实验和资料回答下列问题:
由现象(1)推知X为(写化学式,下同)_______________,
反应②的化学方程式
__________________________________________;
由现象(2)推知X为_______________,反应①的化学方程式为
________________ _________________________;
由现象(3)推知X为__________________________。
无色溶液中溶质的化学式为
__________________ _________。
含钠元素的某白色固体X易溶于水,取少量溶液进行如下实验:
 |
据以上实验和资料回答下列问题:
由现象(1)推知X为(写化学式,下同)_______________,
反应②的化学方程式
__________________________________________;
由现象(2)推知X为_______________,反应①的化学方程式为
________________ _________________________;
由现象(3)推知X为__________________________。
无色溶液中溶质的化学式为
__________________ _________。
“用双氧水和二氧化锰制氧气”的反应方程式为: 。某同学做了该实验后,展开了下列思考与探究:
(1)催化剂MnO2的用量对反应速率有没有影响呢?
他做了这样一组实验:每次均用30mL10%的H2O2溶液,采用不同量MnO2粉末做催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
| MnO2粉末用量(克) | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
| 所用时间(秒) | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
请分析表中数据回答:MnO2的用量对反应速率有没有影响呢?如果有,是怎样影响的呢?
答: 。
(2)H2O2溶液的溶质质量分数对反应速率有没有影响呢?他又做了一组实验:每次均取5mL30%的H2O2溶液,然后稀释成不同溶质质量分数溶液进行实验。记录数据如下:(实验均在20℃室温下进行,其他实验条件也均相同)
| 实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| H2O2溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% | 20% | 25% | 30% |
| MnO2粉末用量(克) | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 | 0.2 |
| 收集到540mL气体时所用时间(秒) | 660 | 220 | 205 | 80 | 25 | 9 | 4 | 3 |
| 反应后液体温度(℃) | 24 | 34 | 39 | 56 | 65 | 67 | 69 | 70 |
请分析表中数据回答:H2O2溶液的溶质质量分数对反应速率有没有影响呢?如果有,是怎样影响的呢?
答: 。
由表中数据还可看出,该反应是个 反应(填“放热”或“吸热”)。
(3)还有哪些因素可能影响该反应的速率呢?
请说出你的一个猜想: 。
由于MnO2和CuSO4溶液都能作H2O2溶液分解的催化剂,某校化学兴趣小组想探究其他一些金属氧化物和盐溶液是否也可以作H2O2溶液分解的催化剂?请你参与他们的探究过程。
(1)[小华的猜想]:Al2O3能作过氧化氢分解的催化剂。
[小明的猜想]:FeCl3溶液能作过氧化氢分解的催化剂。
(2)[实验验证]:
| 实验步骤 | 实验现象 | 实验结论 | |
| 小华的实验 | 将带火星的木条伸入装有过氧化氢溶液的试管中 | 木条不复燃 |
|
|
| 木条复燃 | Al2O3能加快H2O2溶液的分解速率 | |
| 小明的实验 | 在一支试管中加入H2O2溶液,然后滴入适量的FeCl3溶液,把带火星的木条伸入试管。 |
| FeCl3溶液加快H2O2溶液的分解速率 |
(3)[结论]:故Al2O3、FeCl3溶液能作H2O2溶液分解的催化剂。
(4)[反思1]:有的同学认为小华的实验,不能完全证明Al2O3在H2O2溶液分解中起了催化作用。还应补充再探究Al2O3 。
[反思2]:已知FeCl3在水中可解离出Fe3+ 和Cl-,同学们提出以下猜想:
甲同学的猜想是;真正催化分解H2O2的是FeCl3溶液中的H2O;
乙同学的猜想是;真正催化分解H2O2的是FeCl3溶液中的Fe3+;
丙同学的猜想是;真正催化分解H2O2的是FeCl3溶液中的Cl-;
你认为最不可能的是 同学的猜想, 理由是
(5)同学们对余下的两个猜想,用实验进行了探究。请你仔细分析后填表:
| 实验过程 | 实验现象 | 结论 |
| 向盛有5ml5%的H2O2溶液的试管中加入少量 的HCl,并把带火星的木条伸入试管。 | 无明显现象 |
|
| 向盛有5ml5%的H2O2溶液的试管中加入少量 的 ,并把带火星的木条伸入试管。 |
|
|
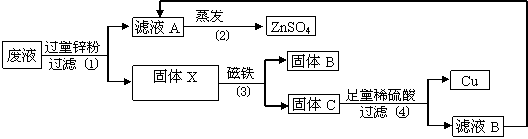
据报载,目前珠江三角洲许多水域和土壤中的重金属含量严重超标,这些重金属对人们的身体健康构成了很大的威胁。某学校学习小组拟从含有大量硫酸亚铁、少量硫酸铜以及不溶性杂质的工业废水中回收金属铜并获得硫酸亚铁晶体。请你协助填写有关空格。
| 操 作 步 骤 | 目 的 |
| ①将废水过滤 | ① |
| ②向滤液中加入过量铁粉 | ② |
| ③ | ③将Cu和过量的铁粉与FeSO4溶液分离 |
| ④在过滤后的固体混合物中加入过量稀硫酸 | ④ |
| ⑤将反应后的混合物过滤 | ⑤ |
| ⑥ | ⑥得到硫酸亚铁晶体 |
(1)操作步骤和目的如下:
(2)写出步骤②和步骤④的化学方程式: 、
。
(3)步骤②中,加入的铁粉刚好反应完后,继续加入的铁粉对最后得到的铜和硫酸亚铁晶体质量的影响分别是(填增大、减小或不变):铜的质量 ;硫酸亚铁晶体质量 。