海水是一种重要的自然资源。以下是对海水资源的部分利用。
(1)从海水中获取淡水。常用的操作方法是 。
(2)从海水中提取溴。从海水中提取的溴约占世界溴产量的![]() ,工业上常用“吹出法”制溴,主要化学原理是2NaBr+C12=2NaCl+Br2,其反应类型是 。
,工业上常用“吹出法”制溴,主要化学原理是2NaBr+C12=2NaCl+Br2,其反应类型是 。
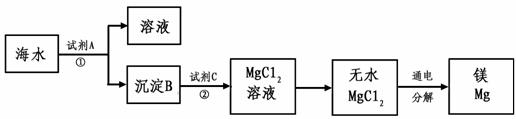
(3)从海水中得到金属镁。下图是从海水中提取镁的简单流程。
上述过程中,沉淀B与试剂C发生的是中和反应,则沉淀B的化学式为 ,由无水MgCl2制取Mg的化学方程式为 。
(4) 从海水中获得氯化钠。将海水进行 可得到粗盐;为除去粗盐中含有
的SO42-、Ca2+、Mg2+等杂质,有如下操作:①溶解;②加过量的Na2CO3溶液; ③加过量的BaCl2溶液;④加适量的盐酸;⑤加过量NaOH溶液;⑥蒸发结晶;⑦过滤。正确的操作顺序是 。(用序号填一种合理组合)。
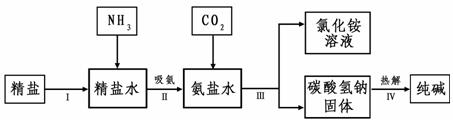 |
(5)海水“制碱”。下图是海水“制碱”的部分简单流程。
制氨盐水的过程中要先通入氨气,再通入二氧化碳。如果反过来,二氧化碳的吸收率会降低。这是因为 。
步骤Ⅳ反应的化学方程式为:
(1)实验室中有一瓶敞口放置的浓盐酸。它的质量分数和放置天数的关系如图1。假设水不蒸发,分析浓盐酸的溶质质量分数变化的原因 。
(2)观察图2,向小试管内滴加水后,可观察到的现象是 。解释产生此现象的原因 。
 |
(3)图3图4分别是溴化氢(HBr)和乙醇(C2H5OH)在水中的微观示意图。请你结合已有的酸、碱知识,判断溴化氢的水溶液显 (填“酸性”、“中性”或“碱性”下同),乙醇的水溶液显 。
(4)向盛有10mL稀盐酸(其中滴有少量指示剂)的烧杯中加入氢氧化钠溶液,用pH计测定溶液的pH,所得数据如下。请分析并回答下列问题:
| 加入NaOH溶液的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
| 烧杯中溶液的pH | 1.1 | 1.2 | 1.4 | 1.6 | 2.5 | 7.0 | 11.0 | 12.0 |
①写出稀盐酸和氢氧化钠溶液反应的化学方程式 。
②若滴加的指示剂是紫色石蕊溶液,当加入氢氧化钠溶液的体积为13mL时,溶液显 色。
③若滴加的指示剂是无色酚酞溶液,加入氢氧化钠溶液充分振荡后,溶液颜色无变化。此时溶液中的溶质一定有(填化学式) 。
小强同学在化学氧自救器的说明书中看到“人呼出气体中的二氧化碳与自救器药罐中的生氧剂(超氧化钾KO2)接触能产生氧气后,对自救器内发生的化学反应原理产生了探究欲望。在老师指导下,小强与同学们展开了以下两个实验探究活动,请你参与。
活动Ⅰ:用下图所示的由a、b、c、d组合成的成套装置和有关药品制取并收集氧气。
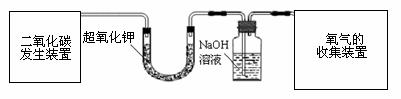
a b c d
(1)用石灰石与稀盐酸制取二氧化碳,则a装置可采用下图中的 (填序号),有关反应的化学方程式为 。
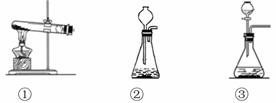 |
(2)用c装置中的氢氧化钠溶液吸收未与超氧化钾反应的二氧化碳。请写出氢氧化钠与二氧化碳反应的化学方程式 。
(3)用 法收集氧气,该收集方法是根据氧气 的性质而确定的。证明生成的气体是氧气,使用 进行检验。
活动Ⅱ:探究二氧化碳与超氧化钾反应除生成氧气外,还生成其它什么物质?
[老师提示]二氧化碳与超氧化钾反应的生成物只有两种,其一是氧气,其二是一种化合物。
[作出猜想]二氧化碳与超氧化钾反应生成的化合物到底是哪种物质?小强作出了以下三种猜想:①是一种酸; ②是一种碱; ③是一种碳酸盐。
通过对反应物有关的元素组成的分析,小影同学认为猜想 、 (填序号)一定是错误的,理由是 。
[进行实验]同学们通过以下实验验证小强同学的另一个猜想。
| 实验步骤 | 实验现象 | 实验结论 |
| 将二氧化碳与超氧化钾反应后的固体加入 |
| 二氧化碳与超氧化钾反应生成的化合物是 (填名称)。 |
[交流与讨论](1)小英认为:二氧化碳与超氧化钾反应的化学方程式 。