0 42513 42521 42527 42531 42537 42539 42543 42549 42551 42557 42563 42567 42569 42573 42579 42581 42587 42591 42593 42597 42599 42603 42605 42607 42608 42609 42611 42612 42613 42615 42617 42621 42623 42627 42629 42633 42639 42641 42647 42651 42653 42657 42663 42669 42671 42677 42681 42683 42689 42693 42699 42707 211419
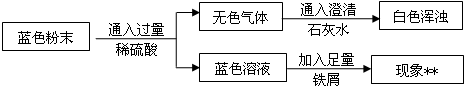
 A、B、C、D、E 分别是铁、氧气、二氧化碳、硫酸铜溶液和氢氧化钠溶液中的一种物质.两圆相交表示两种物质可以发生化学反应,“→”A物质可以一步反应转化为E.下列说法不正确的是( )
A、B、C、D、E 分别是铁、氧气、二氧化碳、硫酸铜溶液和氢氧化钠溶液中的一种物质.两圆相交表示两种物质可以发生化学反应,“→”A物质可以一步反应转化为E.下列说法不正确的是( )
