0 37509 37517 37523 37527 37533 37535 37539 37545 37547 37553 37559 37563 37565 37569 37575 37577 37583 37587 37589 37593 37595 37599 37601 37603 37604 37605 37607 37608 37609 37611 37613 37617 37619 37623 37625 37629 37635 37637 37643 37647 37649 37653 37659 37665 37667 37673 37677 37679 37685 37689 37695 37703 211419
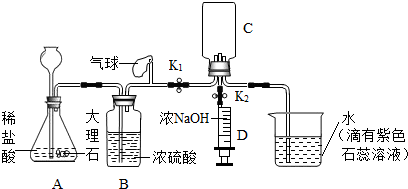
 (2013?佛山)如图,A、B、C、D、E是初中化学中常见的物质,转化关系(其中部分生成物和反应条件已忽略):已知B是黑色固体、相对分子质量为80,E是天然气的主要成份.请回答下列问题:(1)B是
(2013?佛山)如图,A、B、C、D、E是初中化学中常见的物质,转化关系(其中部分生成物和反应条件已忽略):已知B是黑色固体、相对分子质量为80,E是天然气的主要成份.请回答下列问题:(1)B是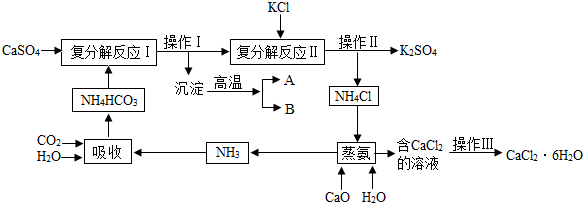
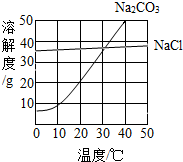 (2013?佛山)如图为氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题;
(2013?佛山)如图为氯化钠、碳酸钠在水中的溶解度曲线.请回答下列问题;