0 36816 36824 36830 36834 36840 36842 36846 36852 36854 36860 36866 36870 36872 36876 36882 36884 36890 36894 36896 36900 36902 36906 36908 36910 36911 36912 36914 36915 36916 36918 36920 36924 36926 36930 36932 36936 36942 36944 36950 36954 36956 36960 36966 36972 36974 36980 36984 36986 36992 36996 37002 37010 211419

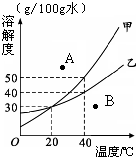 (2011?静安区二模)如图是某实验小组绘制的甲乙两种固体物质的溶解度曲线图.请你根据图示回答问题:
(2011?静安区二模)如图是某实验小组绘制的甲乙两种固体物质的溶解度曲线图.请你根据图示回答问题:
 如图,U形管中是滴有酚酞试液的蒸馏水.向左、右两管中分别同时逐滴滴加一定量
如图,U形管中是滴有酚酞试液的蒸馏水.向左、右两管中分别同时逐滴滴加一定量