0 35252 35260 35266 35270 35276 35278 35282 35288 35290 35296 35302 35306 35308 35312 35318 35320 35326 35330 35332 35336 35338 35342 35344 35346 35347 35348 35350 35351 35352 35354 35356 35360 35362 35366 35368 35372 35378 35380 35386 35390 35392 35396 35402 35408 35410 35416 35420 35422 35428 35432 35438 35446 211419
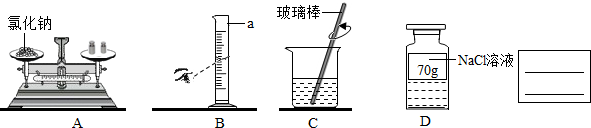

 (2013?重庆模拟)如图是A、B、C三种固体物质的溶解度曲线,根据该图回答下列问题:
(2013?重庆模拟)如图是A、B、C三种固体物质的溶解度曲线,根据该图回答下列问题: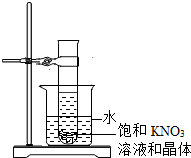 (2013?重庆模拟)某温度下,向盛有几小粒KNO3晶体的试管中,加入10g、10% KNO3的饱和溶液甲,并固定在盛有水的烧杯中(如图所示).向烧杯中加入某种物质后并搅拌,试管中的晶体消失了,得到KNO3 的溶液乙.
(2013?重庆模拟)某温度下,向盛有几小粒KNO3晶体的试管中,加入10g、10% KNO3的饱和溶液甲,并固定在盛有水的烧杯中(如图所示).向烧杯中加入某种物质后并搅拌,试管中的晶体消失了,得到KNO3 的溶液乙.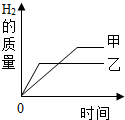 (2012?湘潭)将质量相等的甲、乙两块金属,分别放入质量和溶质质量分数均相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(反应后无固体残余).下列分析正确的是( )
(2012?湘潭)将质量相等的甲、乙两块金属,分别放入质量和溶质质量分数均相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(反应后无固体残余).下列分析正确的是( )