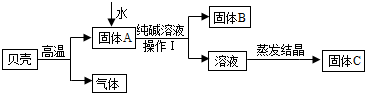
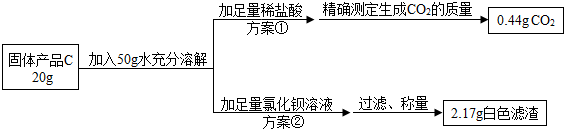
0 34394 34402 34408 34412 34418 34420 34424 34430 34432 34438 34444 34448 34450 34454 34460 34462 34468 34472 34474 34478 34480 34484 34486 34488 34489 34490 34492 34493 34494 34496 34498 34502 34504 34508 34510 34514 34520 34522 34528 34532 34534 34538 34544 34550 34552 34558 34562 34564 34570 34574 34580 34588 211419