9、将零散的化学知识梳理、归纳、会使你的头脑变得更聪明.下列归纳中,不全部正确的( )
|
实验室有一瓶氢氧化钠浓溶液,瓶上标签内容如图所示,请你根据标签上提供的数据解答下列问题:
| 氢氧化钠 体积:500mL 化学式:NaOH 相对分子质量:40 密度:1.5 g/cm3 质量分数:50%(1)用20mL氢氧化钠溶液可以配制质量分数为10%的氢氧化钠溶液 (2)利用刚配制好的氢氧化钠除去混有RCl2的NaCl固体(R代表某二价金属).取20g该固体样品,全部溶解在100g水中,再加入刚配制好的溶液80g,混合到恰好完全反应后过滤,得到固体的质量为9.8g. ①题中发生反应的化学方程式为 ②利用已知条件求解反应生成NaCl质量(x)的比例式为 ③R的元素符号是 ④原混合物中NaCl的质量分数为 ⑤向反应后所得溶液中加入173.8g水,则此时溶液中溶质的质量分数是 |
 8、2008年度诺贝尔化学奖获得者美籍华裔钱永健发明的荧光染剂技术,可以观察细胞内钙离子信号.根据如右图所示相关信息,下列关于钙元素的说法中不正确的是( )
8、2008年度诺贝尔化学奖获得者美籍华裔钱永健发明的荧光染剂技术,可以观察细胞内钙离子信号.根据如右图所示相关信息,下列关于钙元素的说法中不正确的是( ) 4、一种红枣醋饮,其中含有一种有机酸(化学式:C4H6O5),具有美容养颜,解酒护肝健胃的重要用途.下列关于红枣醋饮说法中正确的是( )
4、一种红枣醋饮,其中含有一种有机酸(化学式:C4H6O5),具有美容养颜,解酒护肝健胃的重要用途.下列关于红枣醋饮说法中正确的是( ) 、
、 、
、 三种微粒归为一类,下列微粒中可以归入此类的是( )
三种微粒归为一类,下列微粒中可以归入此类的是( )

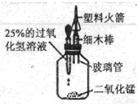 22、某学生利用上述原理设计了如图所示的装置,表演趣味化学实验--“发射火箭”.表演时,挤压胶头滴管时:观察到的现象是
22、某学生利用上述原理设计了如图所示的装置,表演趣味化学实验--“发射火箭”.表演时,挤压胶头滴管时:观察到的现象是
