长久使用的热水瓶底部有一层水垢.为了除去热水瓶底部的水垢,研究性学习小组的同学进行了下列研究和实验:
【查阅资料】水垢的主要成分是CaCO3和Mg(OH)2;Mg(OH)2与盐酸反应化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O.
【实验】取50g水垢的样品(杂质不与盐酸和水反应)放入烧杯中,加入足量的质量分数为10%盐酸,使样品完全反应,并记录反应过程中混合物质量的变化.烧杯及样品和稀盐酸的质量(m)起始时为300g.实验数据记录如下:
【分析与研究】
(1)分析表中记录的数据,你认为反应时间为 min时记录的质量数据是错误的.
(2)Mg(OH)2中镁、氧、氢三种元素的质量比为 .
(3)反应后的混合物中含有CaCl2和MgCl2.9.5g MgCl2含有的氯元素的质量与 g HCl含有的氯元素的质量相当.
(4)水垢中碳酸钙的质量分数是多少?
【查阅资料】水垢的主要成分是CaCO3和Mg(OH)2;Mg(OH)2与盐酸反应化学方程式为Mg(OH)2+2HCl=MgCl2+2H2O.
【实验】取50g水垢的样品(杂质不与盐酸和水反应)放入烧杯中,加入足量的质量分数为10%盐酸,使样品完全反应,并记录反应过程中混合物质量的变化.烧杯及样品和稀盐酸的质量(m)起始时为300g.实验数据记录如下:
| 反应时间(min) | 2 | 4 | 6 | 8 | 10 | 12 | 14 | 16 |
| m(g) | 294.5 | 290.0 | 286.0 | 286.0 | 283.0 | 282.4 | 282.4 | 282.4 |
(1)分析表中记录的数据,你认为反应时间为
(2)Mg(OH)2中镁、氧、氢三种元素的质量比为
(3)反应后的混合物中含有CaCl2和MgCl2.9.5g MgCl2含有的氯元素的质量与
(4)水垢中碳酸钙的质量分数是多少?
下表列出了NH4Cl在不同温度下的溶解度:
(1)10℃时,将20g NH4Cl加入到100g水中,充分搅拌,形成的溶液属于 (填“饱和”或“不饱和”)溶液,该溶液的溶质质量分数为 .
(2)20℃时,向50g水中加入20g NH4Cl,充分搅拌,NH4Cl未能全部溶解,此时该溶液中溶质与溶剂的质量比为 ;要使NH4Cl全部溶解,你的方法是 、 (写出两种方法).
(3)由上表可推出溶解度曲线的变化规律是 .
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 |
| 溶解度/g | 29.4 | 33.3 | 37.2 | 41.4 | 45.8 | 50.4 | 55.2 | 60.2 | 65.6 |
(2)20℃时,向50g水中加入20g NH4Cl,充分搅拌,NH4Cl未能全部溶解,此时该溶液中溶质与溶剂的质量比为
(3)由上表可推出溶解度曲线的变化规律是
在下列空格上填写适当的化学用语或化学用语表示的意义.
(1)氯化钾 ;乙醇
.
(2)能够燃烧,具有还原性和毒性的气体 ;实验室用来制取氧气的紫黑色固体
.
(3)氧化镁中镁元素显+2价 ;2H2O表示
.
(1)氯化钾
(2)能够燃烧,具有还原性和毒性的气体
(3)氧化镁中镁元素显+2价
将15g Cu和Zn的金属混合物粉末加入到一定量的稀硫酸中,恰好完全反应,将所得溶液进行过滤,得到2g固体(滤渣,不含结晶化合物)和200g滤液,则反应后溶液中溶质的质量分数应为( )
| A、6.5% | B、13.9% | C、15.1% | D、16.1% |




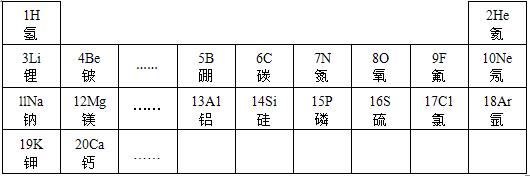
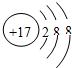 表示的是
表示的是