学校探究小组为了测定市面销售的某品牌纯碱(杂质为NaCl)中碳酸钠的质量分数,进行了如下实验:
①在三个烧杯中都加入1lg样品及足量的水配成溶液;
②向三个烧杯加入质量不同的CaCl2粉末;(化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl)
③将充分反应后生成的沉淀过滤、洗涤、干燥得到w g的白色同体.实验数据如下:
回答下列问题:
(1)碳酸钠中钠、碳、氧三种元素的质量比(最简比)为 .
(2)将烧杯IlI的滤液蒸干,得到 g固体,该固体由 和 (只填化学式)组成.
(3)样品中碳酸钠的质量分数是多少?
①在三个烧杯中都加入1lg样品及足量的水配成溶液;
②向三个烧杯加入质量不同的CaCl2粉末;(化学方程式为Na2CO3+CaCl2═CaCO3↓+2NaCl)
③将充分反应后生成的沉淀过滤、洗涤、干燥得到w g的白色同体.实验数据如下:
| 烧杯Ⅰ | 烧杯Ⅱ | 烧杯Ⅲ | |
| 加入CaCl2的质量/g | 5.55 | 12 | 15 |
| W/g | 5 | 10 | 10 |
(1)碳酸钠中钠、碳、氧三种元素的质量比(最简比)为
(2)将烧杯IlI的滤液蒸干,得到
(3)样品中碳酸钠的质量分数是多少?
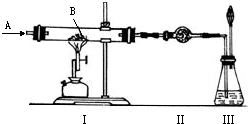
如图所示实验,A为一种无色、无刺激性气味的气体,装置Ⅰ硬质玻璃管中装有1.60克红色粉末B,A、B均属纯净物.有关实验内容如下:
(1)若将所得黑色粉末加入足量稀硫酸中,可生成H20.04克,同时生成一种盐RSO4,则R的相对
原子质量是 .
(2)硬质玻璃管中发生反应的化学方程式是 .
(3)反应后,装置Ⅲ内的液体除沉淀物外,还有的物质是 .
(4)装置Ⅲ处由尖咀管排出的气体,要点火引燃的原因是 .
0 30858 30866 30872 30876 30882 30884 30888 30894 30896 30902 30908 30912 30914 30918 30924 30926 30932 30936 30938 30942 30944 30948 30950 30952 30953 30954 30956 30957 30958 30960 30962 30966 30968 30972 30974 30978 30984 30986 30992 30996 30998 31002 31008 31014 31016 31022 31026 31028 31034 31038 31044 31052 211419

| 实验内容 | 现象 | 测定结果 |
| ①使A持续地通过实验装置Ⅰ、Ⅱ、Ⅲ | Ⅰ中红色粉末逐渐全部变黑 | Ⅰ中产生的黑色粉末的质量为1.12克 |
| ②当A和B在加热下反应时 | Ⅱ中干燥管里的无水CuSO4无变化 | |
| ③实验完毕时,先移去并熄灭酒精灯,冷至室温后,再停止通A | Ⅲ中澄清石灰水变浑浊 | Ⅲ中沉淀1.00克 |
原子质量是
(2)硬质玻璃管中发生反应的化学方程式是
(3)反应后,装置Ⅲ内的液体除沉淀物外,还有的物质是
(4)装置Ⅲ处由尖咀管排出的气体,要点火引燃的原因是

 8、下列为四种粒子的结构示意图,下列说法不正确的是( )
8、下列为四种粒子的结构示意图,下列说法不正确的是( )