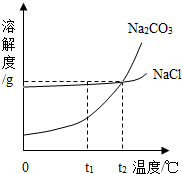
 我国某地区有一种“冬天捞碱,夏天晒盐”的传统.这里的“碱”是指Na2CO3,“盐”是指NaCl.这样捞得的“碱”中会含有少量NaCl.下图为Na2CO3和NaCl的溶解度曲线和部分温度下的溶解度表(单位是克),看图回答下列问题:
我国某地区有一种“冬天捞碱,夏天晒盐”的传统.这里的“碱”是指Na2CO3,“盐”是指NaCl.这样捞得的“碱”中会含有少量NaCl.下图为Na2CO3和NaCl的溶解度曲线和部分温度下的溶解度表(单位是克),看图回答下列问题:(1)①t1℃时,NaCl的溶解度
②“冬天捞碱”的原因是由于Na2CO3的溶解度随温度降低而
③“夏天晒盐”是利用
A.利用风吹日晒,使溶剂蒸发 B.升高温度,使NaCl溶解度增大
(2)根据下表分析:
| 温度 物质 |
0℃ | 10℃ | 20℃ | 30℃ | 40℃ |
| NaCl | 35.7 | 35.8 | 36.0 | 36.3 | 36.6 |
| Na2CO3 | 7.0 | 12.5 | 21.5 | 39.0 | 49.0 |
②下列几种说法中,正确的是
A.碳酸钠晶体的溶解度受温度影响较大
B.将含水各1OOg的氯化钠与碳酸钠的饱和溶液,从30℃降至O℃,析出晶体的质量相等 C.t2对应的温度在2O℃-30℃之间
D.欲从含有少量NaCl杂质的碳酸钠浓溶液中分离出碳酸钠晶体,应采取降低溶液温度的方式.
日常生活中注意膳食合理、营养均衡对人体健康很重要.
(1)下表为某品牌燕麦片标签中的一部分.
燕麦片的营养成分中,人体所需能量的70%左右来自于 ;可以提高人体的免疫力,预防坏血病的发生的是 ;属于人体必需的微量元素是 .(填名称)
(2)下表是王晓明同学体检化验报告单中的部分内容.
对比表中化验“结果”与“参考值”的数据,你能发现王晓明体内 元素指标偏低,这可能会引起的疾病是 (填序号).
A.佝偻病 B.贫血 C.坏血病 D.甲状腺肿大
(3)添加了营养剂的“铁强化”酱油已经面市.根据卫生部的标准,每100mL酱油中铁营养剂添加量是200mg,其中铁元素质量分数为12.5%.酱油中的铁只有10%能被人体吸收,如果食用16mL该酱油,能从酱油中吸收的铁元素为 mg(最后结果保留一位小数).
0 30687 30695 30701 30705 30711 30713 30717 30723 30725 30731 30737 30741 30743 30747 30753 30755 30761 30765 30767 30771 30773 30777 30779 30781 30782 30783 30785 30786 30787 30789 30791 30795 30797 30801 30803 30807 30813 30815 30821 30825 30827 30831 30837 30843 30845 30851 30855 30857 30863 30867 30873 30881 211419
(1)下表为某品牌燕麦片标签中的一部分.
| 每100g含有 营养成分 |
糖类 | 油脂 | 蛋白质 | 维生素C | 钙 | 钠 | 锌 |
| 7.6g | 7.8g | 7.4g | 18mg | 201mg | 30.8mg | 8.1mg |
(2)下表是王晓明同学体检化验报告单中的部分内容.
| 姓名:王晓明 性别:男 年龄:15 | |||
| 编号 | 项目 | 结果 | 参考值 |
| 1 | 血清钾 | 4.15 | 3.50~5.50 |
| 2 | 血清钠 | 145.4 | 135.5~145.0 |
| 3 | 血清氯 | 100.7 | 95.0~108.0 |
| 4 | 钙 | 1.94 | 2.10~2.26 |
| 5 | 磷 | 0.55 | 0.18~1.55 |
| 6 | 镁 | 0.75 | 0.65~1.25 |
A.佝偻病 B.贫血 C.坏血病 D.甲状腺肿大

(3)添加了营养剂的“铁强化”酱油已经面市.根据卫生部的标准,每100mL酱油中铁营养剂添加量是200mg,其中铁元素质量分数为12.5%.酱油中的铁只有10%能被人体吸收,如果食用16mL该酱油,能从酱油中吸收的铁元素为


 实验,得到图2中曲线c.
实验,得到图2中曲线c.



