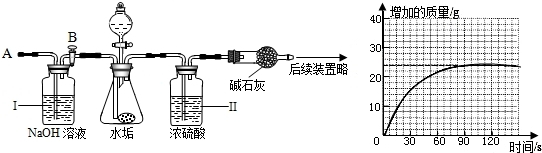
0 28362 28370 28376 28380 28386 28388 28392 28398 28400 28406 28412 28416 28418 28422 28428 28430 28436 28440 28442 28446 28448 28452 28454 28456 28457 28458 28460 28461 28462 28464 28466 28470 28472 28476 28478 28482 28488 28490 28496 28500 28502 28506 28512 28518 28520 28526 28530 28532 28538 28542 28548 28556 211419