已知金属元素M(只有一种化合价)氧化物的化学式为M2O3,则它的硝酸盐的化学式为( )
| A、M(NO3)2 | B、M(NO3)3 | C、MNO3 | D、M2(NO3)3 |
下列化学反应中,属于分解反应的是( )
A、CaCO3
| ||||
| B、Fe+CuSO4=FeSO4+Cu | ||||
C、4P+5O2
| ||||
| D、Na2CO3+Ca(OH)2=CaCO3↓+2NaOH |
某纺织厂为了除去棉麻原料中的非纤维素,可用一定溶质的质量分数的碳酸钠溶液煮沸棉麻原料.现需要80kg20%的碳酸钠溶液.
(1)若用碳酸钠固体和水配制上述溶液,需要碳酸钠的质量是 kg;水的质量是 kg.
(2)甲乙两组同学分别用不同的方案,探究所配得的溶液中碳酸钠的质量分数是否为20%,设计并完成了以下实验:
请用计算结果填空.
①甲组实验1中产生气体的质量是 g;
②依据甲乙两组的数据分别计算所配得的溶液中碳酸钠的质量分数;
甲: ; 乙: .(精确到0.1%)
测定结果与20%之间产生差异可能是实验原理、操作过程等因素引起的.
0 26710 26718 26724 26728 26734 26736 26740 26746 26748 26754 26760 26764 26766 26770 26776 26778 26784 26788 26790 26794 26796 26800 26802 26804 26805 26806 26808 26809 26810 26812 26814 26818 26820 26824 26826 26830 26836 26838 26844 26848 26850 26854 26860 26866 26868 26874 26878 26880 26886 26890 26896 26904 211419
(1)若用碳酸钠固体和水配制上述溶液,需要碳酸钠的质量是
(2)甲乙两组同学分别用不同的方案,探究所配得的溶液中碳酸钠的质量分数是否为20%,设计并完成了以下实验:
| 甲组 | 乙组 | |||||||||||||||||
| 实验过程 | I.取质量是100g的三个烧杯,各盛20g所配得的碳酸钠溶液. II.向三个烧杯中分别放入溶质质量分数相同,但溶液质量不同的盐酸溶液; III.充分反应后再分别称量烧杯及剩余溶液; |
I.取质量是100g的一个烧杯,盛20g所配得的碳酸钠溶液. II.向三个烧杯中滴入溶质质量分数为20%的氯化钙溶液,直到不再产生沉淀为止,过滤、洗涤、晾干、称重; III.绘制加入氯化钙溶液与产生沉淀的质量关系如下图; | ||||||||||||||||
| 所得的数据或关系图 |
|
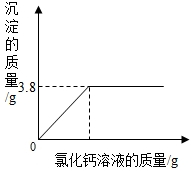 已知发生反应的化学方程式为: Na2CO3+CaCl2═CaCO3↓+2NaCl |
①甲组实验1中产生气体的质量是
②依据甲乙两组的数据分别计算所配得的溶液中碳酸钠的质量分数;
甲:
测定结果与20%之间产生差异可能是实验原理、操作过程等因素引起的.

 14、(1)右图是电解水的装置,通电一段时间后,b试管中收集到的气体是
14、(1)右图是电解水的装置,通电一段时间后,b试管中收集到的气体是