0 26599 26607 26613 26617 26623 26625 26629 26635 26637 26643 26649 26653 26655 26659 26665 26667 26673 26677 26679 26683 26685 26689 26691 26693 26694 26695 26697 26698 26699 26701 26703 26707 26709 26713 26715 26719 26725 26727 26733 26737 26739 26743 26749 26755 26757 26763 26767 26769 26775 26779 26785 26793 211419


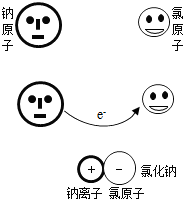 微粒模型观察与比较.如右图所示,在钠与氯气的反应中,每个钠原子失去1个电子,成为1个钠离子;每个氯原子得到1个电子,成为1个氯离子;钠离子与氯离子结合形成氯化钠.因为1个电子的质量大约为1个质子或中子质量的
微粒模型观察与比较.如右图所示,在钠与氯气的反应中,每个钠原子失去1个电子,成为1个钠离子;每个氯原子得到1个电子,成为1个氯离子;钠离子与氯离子结合形成氯化钠.因为1个电子的质量大约为1个质子或中子质量的