阳光牌小包装“脱氧剂”成分为Fe粉、活性炭及少量NaCl、水.使用一段时间后,其中的Fe粉会转变成Fe2O3而变质.某化学兴趣小组欲探究使用过的阳光牌“脱氧剂”的变质程度(已变质的Fe粉占变质前Fe粉的质量分数),设计并进行如下探究过程.
[收集资料](1)Fe(OH)2在空气中可氧化成Fe(OH)3;
(2)难溶性碱受热不稳定,可生成相应的金属氧化物.
[实验探究]
[数据处理]请计算:该“脱氧剂”的变质程度 (⑥).
0 26576 26584 26590 26594 26600 26602 26606 26612 26614 26620 26626 26630 26632 26636 26642 26644 26650 26654 26656 26660 26662 26666 26668 26670 26671 26672 26674 26675 26676 26678 26680 26684 26686 26690 26692 26696 26702 26704 26710 26714 26716 26720 26726 26732 26734 26740 26744 26746 26752 26756 26762 26770 211419
[收集资料](1)Fe(OH)2在空气中可氧化成Fe(OH)3;
(2)难溶性碱受热不稳定,可生成相应的金属氧化物.
[实验探究]
| 实 验 操 作 | 实 验 现 象 | 实 验 结 论 |
| ①取食品包装袋中的“脱氧剂”一袋,将里面的固体溶于水,过滤、洗涤、干燥滤渣. | 无 | 无 |
| ②取步骤①中的滤渣8.0 g,加入足量② |
若没有气泡产生. | 证明固体① |
| 若③ |
证明固体肯定含有④ | |
| ③取步骤②中的滤液,加入足量的NaOH溶液,得到的固体经洗涤后转移到坩埚中,充分加热、冷却、称量,得到8.0 g Fe2O3(注:滤液中的Fe元素已全部转化为Fe2O3) | 无 | 确认固体含有⑤ |

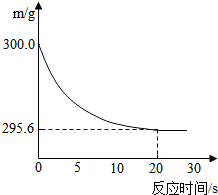 向盛有22.3 g Na2CO3和NaCl固体混合物的烧杯中加入216.1 g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如下图所示:烧杯连同药品的起始质量为300 g.回答下列问题:
向盛有22.3 g Na2CO3和NaCl固体混合物的烧杯中加入216.1 g稀盐酸恰好反应,反应过程用精密仪器测得烧杯连同药品的质量(m)与反应时间(t)的关系如下图所示:烧杯连同药品的起始质量为300 g.回答下列问题:



