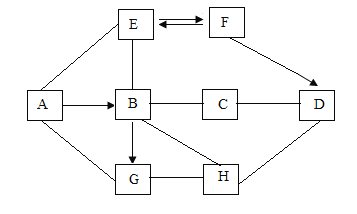
【题目】学习完酸碱盐的知识后,某化学兴趣小组同学在实验室做如图所示实验,小明取2mLNa2CO3溶液于试管中,滴入少量稀盐酸,无明显现象(如图1);小英取2mL稀盐酸于试管中,滴入少量Na2CO3溶液,却观察到立即有气泡产生(如图2)。两人实验所用的Na2CO3溶液、稀盐酸均相同,却观察到不同的实验现象,为此,他们进行了如下探究。
(提出问题)小明实验后溶液中的溶质是什么?
(作出猜想)①NaCl;②NaCl、 NaHCO3;③ NaCl Na2CO3;④NaCl、Na2CO3 NaHCO3
(查阅资料)
a.HCl和Na2CO3反应是分步进行的,即:
![]()
![]() (后)。
(后)。
说明上述猜想__________一定不成立(填序号);
b. NaHCO3溶液与足量澄清石灰水混合会变浑浊;
c.Ca(HCO3)2溶于水。
(实验探究)
实验操作 | 实验现象 | 结论 |
取适量小明实验后的溶液于试管中滴入澄清石灰水 | 溶液变浑浊 | 猜想④成立 |
(交流反思)(1)请分析上述实验探究结论是否正确,并说明原因________________________________。
(2)请设计一个实验来验证剩余猜想。
实验操作 | 实验现象 | 结论 |
猜想______成立 |
(归纳总结)小明实验与小英实验现象不同的主要原因为________________________________。
【题目】氢氧化钡可用作杀虫剂。实验室中有一瓶含有少量氢氧化钠的氢氧化钡样品,某化学兴趣小组的同学为测定该样品中氢氧化钡的质量分数,进行了以下实验:分别取120 g样品,平均分成6份加入烧杯中,分别加入80g水溶解,再加入碳酸钠溶液充分反应,对反应后的混合物进行如图所示的操作:
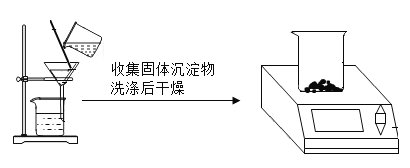
测得六组实验数据如下表所示,试计算:(钡的相对原子质量为137)
实验组数 | 第一组 | 第二组 | 第三组 | 第四组 | 第五组 | 第六组 |
加入碳酸钠溶液的质量/g | 25 | 50 | 75 | 100 | 125 | 150 |
天平示数/g | 3.94 | 7.88 | 11.82 | 15.76 | m | 19.70 |
(1)m的值为______________。
(2)样品中氢氧化钡的质量分数____________。
(3)将恰好反应的液体配制成溶质质量分数为10%的氢氧化钠溶液以便实验室使用,需要再称取____________克氢氧化钠固体?
【题目】已知某黑色粉末可能是由铁粉、氧化亚铁、四氧化三铁的一种或两种组成,某化学兴趣小组为确定黑色粉末的成分进行了如下探究。
[查阅资料]铁的氧化物均能与稀酸反应,且只有四氧化三铁能被磁铁吸引。
[方案设计]
实验操作 | 实验现象 | 实验结论 |
实验一:取适量的黑色粉末,用磁铁吸引 | ______________。 | 黑色固体粉末中一定不含氧化亚铁 |
实验二:_______________。 | 有气泡产生,溶液颜色发生改变 | 黑色固体一定含有铁粉,可能含有四氧化三铁 |
[交流反思]为探究黑色粉末是否含有四氧化三铁,小明认为可将实验二的操作改为取适量黑色固体粉末于试管中,加入足量的硫酸铜溶液,当出现_____________时,可证明黑色固体粉末中一定含有铁粉和四氧化三铁。
[继续探究]为探究黑色粉末成分中铁粉和四氧化三铁的质量比,同学进行了如图实验;反应前称取10g黑色粉末加入玻璃管内(玻璃管的质量为50 g) ,先通入一段时间一氧化碳气体,然后点燃酒精灯。
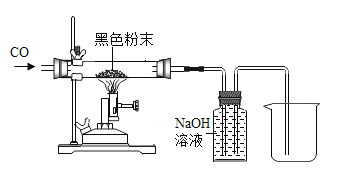
(1)反应前先通入一氧化碳气体再点燃酒精灯,目的是______________。
(2)充分反应后熄灭酒精灯,继续通入一氧化碳,待冷却到室温后停止通入,称量玻璃管和管内固体总质量为58.4g,计算黑色粉末中铁和四氧化三铁的质量比为___________________。
(3)虚线框内的装置的作用是_________________。
【题目】某化学活动小组在一次探究复分解反应的实验活动中,选取了下表中四种化合物的溶液相互反应,它们之间能发生反应但无明显现象的是___________________________(填序号)。
A | B | C | D |
氢氧化钠溶液 | 稀盐酸 | 碳酸钠溶液 | 氯化钡溶液 |
实验结束后,小组同学将废液倒入废液缸中。将废液缸内的物质过滤后,对滤液成分进行了进一步的探究。小组同学经认真分析,推出废液中一定含有Na+、Cl -。欣欣同学按图示取少量废液于试管中滴入无色酚酞试液,发现溶液变红。
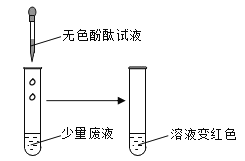
[提出问题]废液缸中的废液中还含有哪些离子?
[猜想与假设]
猜想1:废液中还含有OH-、CO32- ;
猜想2:废液中还含有OH-、Ba2+;
猜想3:废液中还含有CO32- ;
猜想4:废液中还含有 ______________(填离子符号,下同)
[实验探究]
实验操作 | 实验现象 | 实验结论 | |
甲同学 | 取少量废液于试管中,向其中滴加足量稀盐酸 | 观察到有气泡冒出 | 废液中一定含有 _________________________ 。 |
乙同学 | 另取少量废液于试管中,向其中滴加足量 ___________________ ,再滴加无色酚酞试液 | 可观察到溶液中产生白色沉淀 _____________________ 。 | 猜想1成立 |
[讨论交流]甲同学的实验中观察到产生气泡时所发生反应的化学方程式为 ______________________ 。
[评价与反思]在实验探究环节中,加入的试剂均足量,请写出原因 _____________________
【题目】某化工厂用废硫酸制备K2SO4的工艺流程如图所示,根据流程回答相关问题。
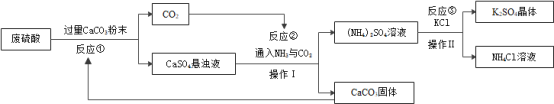
(1)反应①之前将CaCO3研成粉末的目的是______________,反应①的化学方程式为___________。
(2)实验室操作I时要用的一种玻璃仪器是___________。
(3)反应②的化学方程式为![]() ,则X的化学式为________________。
,则X的化学式为________________。
(4)反应③中相关物质的溶解度如下表所示:
物质 | (NH4)2SO4 | KCl | K2SO4 | NH4Cl |
溶解度/g(20° C) | 75.4 | 34.2 | 11.1 | 37.2 |
反应③在常温下能发生的原因是___________。
(5)上述流程中可循环使用的物质是_____________(填化学式)。