【题目】下表是三种物质在不同温度时的溶解度,根据表中提供的信息回答下列问题。
温度/℃ | 0 | 20 | 40 | 60 | 80 |
氯化钠 | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 |
硝酸钾 | 13.3 | 31.6 | 63.9 | 110 | 169 |
熟石灰 | 0.19 | 0.17 | 0.14 | 0.12 | 0.09 |

(1)在上图中自己建立坐标系绘制硝酸钾的溶解度曲线。________________
(2)其饱和溶液随温度升高而析出固体,该物质的化学式为_____________________。
(3)20℃时氯化钠饱和溶液的溶质质量分数为_______________________。
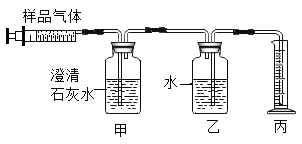
【题目】石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应)。课外小组同学将50g盐酸均分5次加入到20g该石灰石样品中,得到如下部分数据和图象:
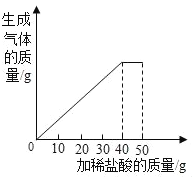
次数 | 第1次 | 第2次 | 第3次 |
加入盐酸的质量/g | 10 | 10 | 10 |
剩余固体的质量/g | 16 | 12 | 8 |
请计算:
(1)石灰石样品中杂质的质量为_____g。
(2)所加盐酸的溶质质量分数_____。
(3)实验室只提供溶质质量分数为36.5%的盐酸,欲配制该实验所用的50克盐酸,需要36.5%的盐酸和水各多少克?_____
【题目】做完氢氧化钠与稀硫酸中和反应的实验后,兴趣小组的同学对反应后溶液中的溶质成分产生了兴趣,请你与他们一起进行以下探究
(提出问题)溶液中的溶质是什么物质?
(作出猜想)(1)甲同学认为溶液中的溶质只有Na2SO4一种物质。
(2)乙同学认为溶液中的溶质是Na2SO4和_____(填化学式)两种物质。
(3)丙同学认为溶液中的溶质是Na2SO4和NaOH两种物质。
(查阅资料)①Na2SO4溶液显中性,
②Al与强碱NaOH溶液反应生成偏铝酸钠(NaAlO2)和氢气。
(实验验证)
实验操作 | 实验现象 | 实验结论 | |
乙同学 | 取反应后的溶液少许于试管中,将表面反复打磨后的铝片放入该溶液中 | 铝片逐渐溶解,并有大量气泡冒出,收集气体点燃,火焰呈淡蓝色 | 猜想(2)成立 |
丙同学 | 取反应后的溶液少许于试管中,向试管中滴加几滴无色酚酞试液 | 溶液由无色变成_____色 | 猜想(3)成立 |
(总结反思)丁同学根据乙、丙两位同学的实验现象,首先肯定猜想(1)不成立,经过进一步分析,丁同学认为猜想(2)也不成立,他的理由是_____。兴趣小组的同学经过充分讨论,一致认为猜想(3)成立。
(知识拓展)(1)取氢氧化钠与稀硫酸反应后的溶液少许于试管中,加入下列_____物质也能证明猜想(3)成立。
A 硫酸铜溶液
B 氯化钡溶液
C 稀盐酸
D 二氧化碳
(2)乙同学的实验中铝片与_____(填化学式)溶液发生了反应,请写出铝与该溶液发生反应的化学方程式_____。