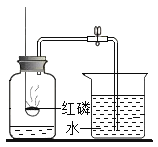
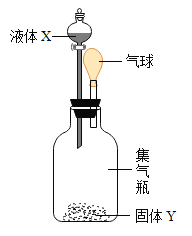
【题目】如图所示,将液体X加入到集气瓶中与固体Y作用,观察到气球逐渐变大,如表中液体X和固体Y的组合,符合题意的是( )
① | ② | ③ | ④ | ⑤ | |
X | 稀盐酸 | 水 | 水 | 双氧水 | 水 |
Y | 铁粉 | 氢氧化钠 | 氯化钠 | 二氧化锰 | 硝酸铵 |
A.①②③④⑤B.①②④C.①③④D.①④⑤
【题目】某小组同学设计并进行实验,探究影响过氧化氢分解速率的因素。(实验装置如图所示,夹持仪器已略去)
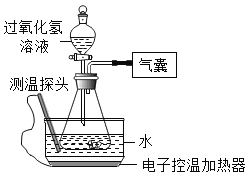
(猜想与假设)
影响过氧化氢分解速率的因素可能有温度、溶液的浓度、催化剂用量。
(实验记录)
同学们进行6组实验,实验记录如下:
实验序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
过氧化氢溶液的 浓度(%) | 30 | 30 | 15 | 30 | 30 | 30 |
过氧化氢溶液的 体积(mL) | 6 | x | 6 | 6 | 6 | 6 |
水槽中水的温度 | 20 | 90 | 70 | 70 | 20 | 20 |
锥形瓶中的物质 | 0.1g MnO2 | 0.5g MnO2 | ||||
6min内产生氧气(mL) | 0.0 | 41.0 | 4.5 | 12.1 | 2.0 | 650.0 |
(解释与结论)
(1)实验②中应加入过氧化氢溶液的体积x是________mL。
(2)实验①-⑥可以通过测定__________来比较过氧化氢的分解速率。
A 相同时间内产生氧气的体积
B 产生相同体积的氧气所需时间
C 相同时间内产生氧气的质量
(3)得出“过氧化氢溶液的浓度越大分解速率越快”结论所依据的实验是____(填序号)。
(4)通过实验①、②、④可得出的结论是_________。
(反思与评价)
(5)同学们认为实验室制氧气,应选择实验⑥而不选实验②的理由是________(答一点即可)