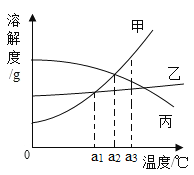
【题目】如下图的加热袋常用于野外加热食物。加热袋中的固体粉末含镁粉、铁粉和氯化钠,使用时向其中加入水袋中的水,即可产生大量热。实验小组针对放热过程中的反应原理展开探究。

(查阅资料)
常温下镁粉能与水发生置换反应,且放热。
(进行实验)
同学们用下图所示装置进行模拟实验:分别取不同成分的固体粉末放入甲中,通过分液漏斗向其中均加入8 mL水,读取甲中所得固液混合物的最高温度,实验记录如下表:
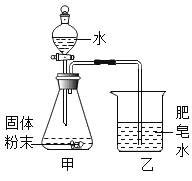
(实验时的室温为22.8℃)
实验序号 | A | B | C | D | E | F |
固体成分 | Mg | Fe | Mg+Fe | Mg+NaCl | Fe+NaCl | Mg+Fe+NaCl |
乙中现象 | 少量肥皂泡,难以点燃 | ? | 少量肥皂泡,难以点燃 | 较多肥皂泡,点燃有爆鸣声 | 无肥皂泡 | 大量肥皂泡,点燃有爆鸣声 |
混合物温度 | 23.1℃ | 22.8℃ | 23.1℃ | 24.2℃ | 22.8℃ | 27.2℃ |
(解释与结论)
(1)实验B,乙中现象为_______________。
(2)实验A证明了镁粉与水能反应,完成该反应的化学方程式Mg+2H2O=____+H2↑
(3)使镁粉与水迅速反应并放热的最佳方法是向镁粉中加入_____________。
(反思改进)
(4)同学们分析实验数据发现,升高的温度没有达到食品加热袋的效果,其可能的原因是___________。
(5)同学们根据实验结果进一步猜测,实验F中的反应结束后,甲中剩余固体混合物中仍然含有铁粉,检验其铁粉存在的的实验方案为:取少量固体混合物___________________。
(6)从上述实验初步得出“NaCl溶于水没有热量的变化”的结论,依据的两个实验是(填实验序号)______________
【题目】某研究性学习小组在验证"铝丝与硫酸铜溶液反应"的实验时,发现很长一段时间铝丝表面都没有明显的现象。
[ 提出问题 ] 是什么原因导致反应现象不明显呢?
[ 查阅资料 ] 氯离子穿透铝表面致密氧化膜的能力强于硫酸根离子。
[ 猜想与假设 ]
甲:可能与反应物间的接触面积有关;
乙:可能与硫酸根离子穿透氧化膜的能力有关;你认为还可能与_________有关( 写出一条即可 )。
[设计实验 ]
(1)将打磨后的等质量的铝片和铝丝分别放入等体积、浓度的硫酸铜溶液中,发现前者反应的速率明显比后者快,观察到的现象是__________。甲认为自己的猜想正确。
(2) 你认为该实验设计是_________(填“严谨" 或“不严谨”)的,理由是________。请写出铝与硫酸铜溶液反应的化学方程式___________。
(3)设计实验验证乙的猜想:
实验操作 | 实验现象 | 实验结论 |
室温下,将两根相同的铝丝分别放入等体积、浓度的硫酸铜溶液和______________溶液中 | 后者铝丝表面变红明显比前者快 | 乙同学猜想正确 |
(4)若要进一步验证乙的猜想,请完成下列实验方案;
实验操作 | 实验现象 | 实验结论 |
_________ | _________ | 乙同学猜想正确 |
【题目】已知白磷的着火点为40℃,某兴趣小组探究可燃物的燃烧条件,实验装置图和实验步骤如下表:(实验过程中长颈漏斗下端始终在液面以下:注射器的摩擦力忽略不计)

实验步骤 | 实验现象 |
①将白磷放在燃烧匙内,塞好胶塞 | |
②从长颈漏斗向瓶内迅速注入60℃的水至刚刚浸没白磷 | 白磷没有燃烧 |
③连接好注射器,向瓶内推入空气,瓶内水面下降,停止推入空气 | 白磷燃烧,有白烟产生 |
④白磷熄灭后,冷却至室温,瓶内水面上升,最后淹没白磷 |
(1) 实验前需要检查装置的气密性,请写出检查该装置气密性的方法________。
(2) 请写出白磷燃烧的化学方程式___________________。
(3) 对比步骤②和③可知,可燃物燃烧的条件之一是___________,若把60℃的水换成20℃水,重复以上实验步骤,还可以得出物质燃烧需要的条件是________
(4) 步骤④中瓶内水面上升的原因是_____。