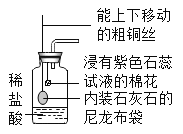
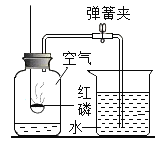
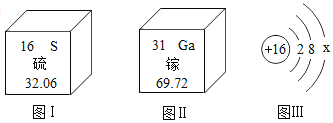
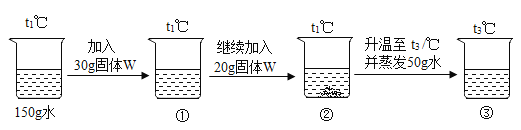
【题目】某化学小组为测定大理石中碳酸钙的含量,称取大理石样品25.0g,分成五等份于5个烧杯中进行实验,记录有关实验数据如下表所示(大理石中其它成分均不溶于水,也不参加反应),计算:
烧杯① | 烧杯② | 烧杯③ | 烧杯④ | 烧杯⑤ | |
加入大理石样品的质量/g | 5.0 | 5.0 | 5.0 | 5.0 | 5.0 |
加入稀盐酸的质量/g | 10.0 | 20.0 | 30.0 | 40.0 | 50.0 |
烧杯中剩余固体的质量/g | 4.0 | 3.0 | 2.0 | 1.0 | 1.0 |
(1)样品中碳酸钙的质量是 。
(2)所用稀盐酸的溶质质量分数。
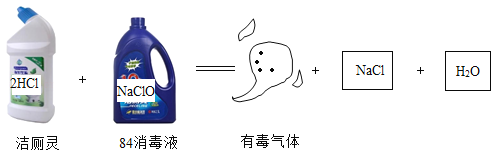
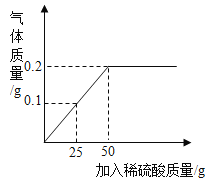
【题目】实验室里有一瓶常用的无色液体试剂,因保管不当造成标签破损(如图所示),其残缺的标签中只剩下“Na”和“10%”字样。小强和小华同学对此很兴趣,决定对其成分进行探究。
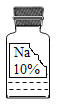
(提出问题)该瓶试剂到底是什么物质的溶液呢?
(查阅资料)I.初中化学中常见的含钠化合物有:NaCl、NaOH、Na2CO3、NaHCO3。
II.Na2CO3和NaHCO3的水溶液都呈碱性。
Ⅲ.测定室温(20C)时,四种物质的溶解度数据如下:
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
溶解度/g | 36 | 109 | 205 | 9.6 |
(得出结论)小华根据试剂瓶标签上标注的溶质质量分数为10%和上表中的溶解度数据判断,这瓶试剂不可能是____溶液。
(作出猜想)①可能是NaCl溶液;②可能是Na2CO3溶液;③可能是_____溶液;
(设计方案并实验)
(1)小强用洁净的玻璃棒蘸取该溶液滴在pH试纸上,测得pH>7,则这瓶试剂不可能是NaCl溶液。
(2)小强为了进一步验证猜想,他又进行了如下实验:
操作步骤 | 实验现象 | 结论 |
①取样品于试管中,滴加_____ | 产生大量气泡 | 猜想②正确 |
②把产生的气体通入澄清石灰水中 | 有白色沉淀产生 |
(拓展与应用)请你选择与小强不同的试剂来验证猜想②成立,你选择____溶液。
【题目】小明同学家新买了铜质镀铬的水龙头,为了了解铬与常见金属铝、铜在金属活动性顺序中的相对位置关系,进行如下探究活动。
(查阅资料)铬(Cr)是银白色有光泽的金属,在空气中表面能生成抗腐蚀性的致密氧化膜。铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
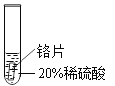
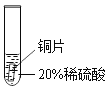
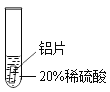
(设计实验)取大小相同的三种金属片,用砂纸打磨光亮,再取三支试管,分别放入等量的同种稀硫酸
实验一 | 实验二 | 实验三 | |
实验方案 |
|
|
|
实验现象 | _____。 | 铝片表面产生气泡较快 | |
结论 | 铬片表面产生气泡缓慢,溶液变蓝色 | 铜不与稀酸反应 | 铝能与稀硫酸反应,反应速率较快 |
三种金属在金属活动性顺序中的相对位置关系是 Al>Cr>Cu | |||
(回答问题)
(1)实验一发生反应的化学方程式是_____。
(2)小刚提出用硫酸铜代替上述实验中的稀硫酸也能得出三种金属在金属活动性顺序中的相对位置关系,小燕认为不可行,理由是_________。
(3)小红认为只要选用三种试剂进行实验就可以得出三种金属在金属活动性顺序中的相对位置关系,这三种试剂可以是_____。