【题目】氨气是无色、密度比空气小、极易溶于水![]() 的刺激性气体,强烈刺激眼睛和黏膜。可用于制造化肥、制冷剂,亦可用于炸药、染料、塑料和一些药物的生产等。请回答下列问题:
的刺激性气体,强烈刺激眼睛和黏膜。可用于制造化肥、制冷剂,亦可用于炸药、染料、塑料和一些药物的生产等。请回答下列问题:
(一)氨气的合成是人类科学技术的重大突破,工业上合成氨的微观示意图如下。
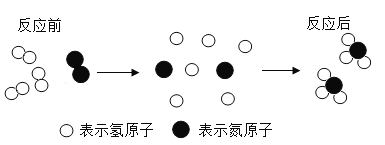
(1)该化学变化过程中不可再分的微粒符号为____________________________。
(2)该反应条件是高温、高压及催化剂,则化学方程式为_________________。
(二)在实验室里,我们可选用下图中所提供的实验装置制取氨气并进行相关实验探究。
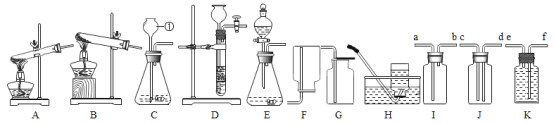
(3)写出标号仪器①的名称___________________________________.
(4)实验室制备氨气是利用氯化铵和熟石灰固体加热来生成,发生反应的化学方程式为____________,选用的装置代码为____________________.其验满的方法是_____________________________________.
(三)天天兴趣小组的同学决定通过实验设计定量研究氨气中氮、氢两种元素的质量比。
(查阅资料)
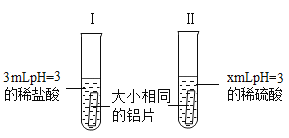
I.![]()
II. ![]() ;
;![]()
III.干燥剂种类:氯化钙、浓硫酸、氢氧化钠、碱石灰、无水硫酸铜等
(方案设计)天天小组同学将产生氨气装置依据设计流程连接成实验探究装置如下图所示。
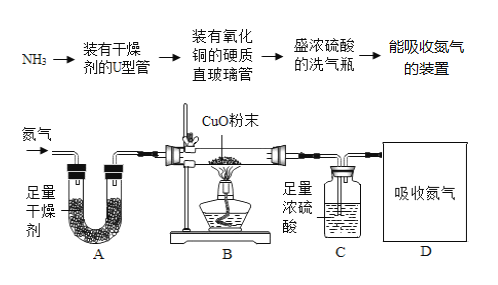
(实验观察)
(5)可作A中U形管内干燥剂的物质是________________________________.
(6)在B装置直玻璃管内出现的现象是____________________________________.
(7)通常把金属氧化物失去氧转化为金属的过程,称为金属氧化物的还原。那么B装置中玻璃管内发生后的还原过程是指_______________________________________________.
(数据分析)待充分反应后,测得A、B、C、D四个装置前后的质量变化如下表所示:
装置编号 | A | B | C | D |
记录数据 | 增加0.1g | 减少4.8g | 增加6.0g | 增加2.8g |
(8)可选择与计算需要数据相应的装置编号为________________________.
(9)通过计算:氮元素质量______________,氢元素质量__________________.列比例式计算氮、氢元素的质量比为____________________________.
【题目】钠及其化合物是中学化学学习和研究的重要内容,以下是对这一知识模块的梳理和认知,请你共同参与。
知识点一、认识钠元素及氯化钠的形成:
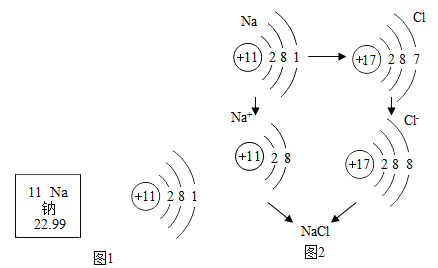
(1)下列是某同学据图1获得的信息,其中正确的是________________(填序号);
①钠元素属于金属元素
②钠的相对原子质量为22.99g
③钠原子在化学反应中易得到电子
④![]() 表示原子核带11个单位正电荷
表示原子核带11个单位正电荷
(2)图2是氯化钠的形成过程,其微观实质是________________________。
(3)由图推测下列说法正确的是(填序号)________________________。
①原子形成离子的过程中,结构中的电子数一定改变
②原子形成离子的过程中,电子层数一定改变
③原子形成离子的过程中,质子数一定不变
④化学变化中元素种类一定不变
知识点二、探究氢氧化钠的化学性质
为验证氢氧化钠的化学性质,设计了如下图所示实验方案:
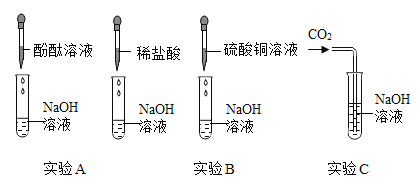
(1)实验A验证了氢氧化钠的两条化学性质,其中酚酞试液所起的作用是________________
(2)实验B中发生反应的化学方程式为_________________________。
(3)实验C没有观察到明显现象,于是他们展开了如下探究:制取纯净、干燥的二氧化碳气体,并验证二氧化碳气体与氢氧化钠溶液可以发生化学反应。
(查阅资料)
①碳酸钠、水、二氧化碳可以化合生成碳酸氢钠。
②20℃,氢氧化钠、碳酸钠和碳酸氢钠的溶解度如下表所示。
物质 | NaOH |
|
|
溶解度/g | 110 | 21.8 | 9.6 |
(定性探究)
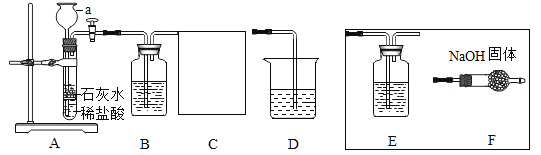
①装置A中发生反应的化学方程式为:____________________________________;
②装置B中盛有![]() 溶液,目的是____________________________________;
溶液,目的是____________________________________;
③图中C处装置应该选择_________(选填E或F)达到实验目的;
④在实验过程中装置D中观察到___________________________,说明![]() 和NaOH溶液能发生反应。
和NaOH溶液能发生反应。
(定量计算)
20℃时,装置D中盛有210g NaOH的饱和溶液,经测定,实验过程中装置D的温度保持20℃。试计算:
⑤装置D中210g NaOH饱和溶液含有NaOH的质量是__________________g;
⑥装置D中NaOH全部转化成![]() 时理论上最多可以生成
时理论上最多可以生成![]() 的质量是_________g;
的质量是_________g;
⑦当向装置D中通入足量的![]() 时,可以将NaOH全部转化为
时,可以将NaOH全部转化为![]() ,实验过程中会析出
,实验过程中会析出![]() 的质量为__________________g(不考虑结晶水)。
的质量为__________________g(不考虑结晶水)。
知识点三、对比碳酸钠和碳酸氢钠的化学性质
(1)比较碳酸钠和碳酸氢钠两种溶液的酸碱性
(查阅资料)
20℃ | 8% | 8% |
pH | 10.6 | 8.0 |
现有20℃时溶质质量分数为8%的![]() 和
和![]() 溶液,由数据可知两种溶液都显____________(填“酸性”、“碱性”或“中性”);这两种物质中常用作治疗胃酸过多的药剂是____________
溶液,由数据可知两种溶液都显____________(填“酸性”、“碱性”或“中性”);这两种物质中常用作治疗胃酸过多的药剂是____________
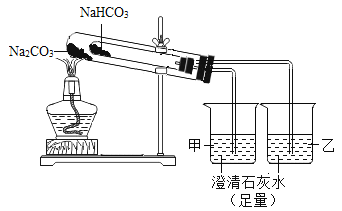
(2)比较碳酸钠和碳酸氢钠的热稳定性:
按图实验,充分加热后,观察到的现象:大试管内固体物质无明显变化,小试管内壁有水珠生成;甲烧杯中石灰水无明显现象,乙烧杯中石灰水变浑浊。试回答
①在实验结束时,操作上要注意的问题是____________________
②由实验可以得出的结论是________________________________