【题目】某实验小组同学在向饱和碳酸钠溶液中逐滴加入稀盐酸时,开始时未观察到气泡。
(提出问题)开始时为什么没有出现气泡?
(查阅资料)碳酸钠溶液与稀盐酸的反应分两步进行:其中第一步反应的化学方程式为Na2CO3+ HCl ═NaCl + NaHCO3,第二步为碳酸氢钠与盐酸反应。
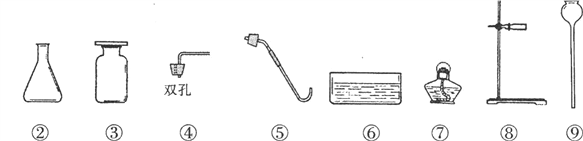
(进行实验一)同学们设计并进行了如下图所示实验(装置气密性良好)。
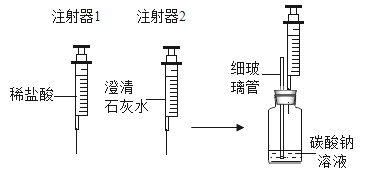
实验 | 操作 | 现象 |
1 | 用注射器1向小药瓶中缓慢注入少量的稀盐酸,边注入边振荡 | 细玻璃管中液柱略微升高 |
换注射器2从瓶中缓慢抽取气体 | 澄清石灰水无明显变化 | |
2 | 用注射器1向小药瓶中继续注入稀盐酸至较多气泡产生 | ________ |
________ | 澄清石灰水变浑浊 |
(1)澄清石灰水变浑浊的化学方程式为____。
(2)实验2中①的现象是____。
(3)实验2中②的操作是____。
(4)细玻璃管在实验中的主要作用是____。
(进行实验二)在老师的帮助下,同学们利用pH传感器对相同浓度的碳酸钠溶液(pH为12)、碳酸氢钠溶液(pH为8.2)与盐酸反应时,pH的变化与盐酸体积的关系进行了测定,并做了如下所示的对比图:
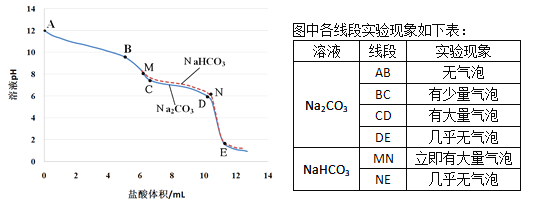
(5)在AB段,溶液中的溶质有____。
(6)分析图表,充分体现碳酸钠与稀盐酸第二步反应的是_______段。
(反思与评价)
(7)若将碳酸钠溶液逐滴滴加到盐酸中,出现的现象是____。