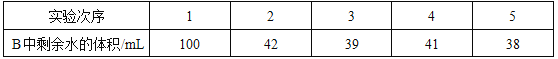
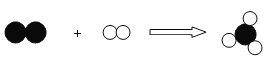【题目】催化剂在生产、生活和科研中的地位越来越重要。
探究一:验证MnO2在过氧化氢分解前后的质量没有改变。
某同学用电子天平称取1.0gMnO2于试管中,加入适量过氧化氢溶液,写出发生反应的化学方程式_____________。反应结束后,过滤、洗涤、称量,发现所得固体质量大于1.0g,其可能原因是____________。小强针对上述原因提出烘干后再称量的方案,结果得到了准确的实验结果。
探究二:温度对过氧化氢反应速率的影响。
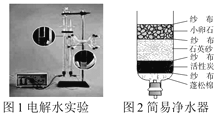
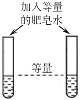
某同学用如图所示装置进行实验,发现加热后产生气泡速率明显加快,但用带火星的木条检验产生的氧气时,木条很难复燃,其可能原因是____________。
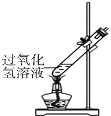
经实验测定,受热液体的温度与得到氧气的体积分数之间存在一定关系(如图所示)。若能使带火星木条复燃所需氧气的体积分数最低为49%(只考虑氧气的体积分数对实验结果的影响),现欲使带火星的木条复燃,应将加热过氧化氢溶液的最高温度控制在_________ ℃以下。
探究三:红砖粉是否也能作过氧化氢分解的催化剂?效果怎样?
小雨以收集等体积的氧气为标准,设计了下列三组实验(其它可能影响实验的因素均忽略)。
编号 | 过氧化氢 | 其他物质 | 待测数据 |
实验1 | 20mL 5% 过氧化氢溶液 | 无 | |
实验2 | 20mL 5% 过氧化氢溶液 | 1g红砖粉 | |
实验3 | 20mL 5% 过氧化氢溶液 | 1g二氧化锰 |
(1)上表中的“待测数据”是_____________。
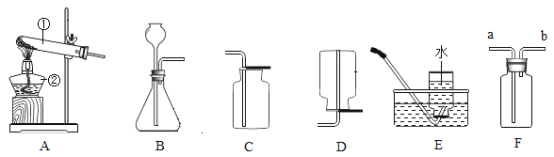
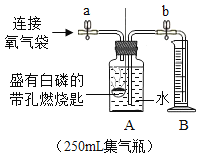
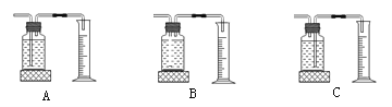
(2)如图可用于此实验收集O2的装置是_________(填字母)。一开始导管排出的气体是否收集?其理由是____________。
(3)通过实验1与实验____________的待测数据对比,可说明红砖粉能改变过氧化氢分解速率。
(4)如需证明红砖粉可作过氧化氢分解的催化剂,还需通过实验证明_______。
【题目】下表是部分元素的原子结构示意图等信息如下,请回答下列问题。

(1)原子序数为10的元素属于____________(填“金属”、“非金属”或“稀有气体”)元素,位于第二周期第ⅣA族的元素的名称是___________。
(2)一种元素与另一种元素间的本质区别是_________,硫元素和氧元素具有相似的化学性质,是因为硫原子和氧原子的___________相同。
(3)与氯离子核外电子层排布相同的原子是___________。
(4)如图所示是元素周期表中铝元素的相关信息。则铝的相对原子质量为___________,其氧化物的化学式为___________。

(5)一般来说,电子层数相同的原子(稀有气体除外),原子半径随着原子序数的递增而逐渐减小;最外层电子数相同的原子,原子半径随电子层数的增加而增大。由此可知:氧原子、钠原子和硫原子的半径由大到小的顺序为_______。
(6)A物质为奥运火炬常用燃料,纯净物A在B物质中充分燃烧,发生反应的化学方程式为:A+ 5B![]() 3C + 4D(部分微观示意图如下所示)。
3C + 4D(部分微观示意图如下所示)。
物质 | A | B | C | D |
|
分子示意图 | ? |
|
|
|
①组成A物质的元素为__________。
②此反应中生成物C、D的质量比为____________。
【题目】化学教材“寻找新的催化剂”研究性实验,引起了化学探究小组的兴趣.
(提出问题)(1)氧化铁(Fe2O3)能否作过氧化氢溶液分解的催化剂?
(2)氧化铁与二氧化锰催化效果哪个好?
(3)催化剂的质量是否对过氧化氢溶液分解的速率产生影响?
(实验探究)
实验步骤 | 实验现象 |
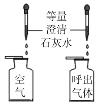
①分别量取5mL15%过氧化氢溶液放入A、B两支试管中,向A试管中加入ag氧化铁粉末,并分别在A、B两支试管中插入带火星的木条,观察现象 | A试管中产生大量气泡,带火星木条复燃, B试管中的现象:…… |
②待A试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管内,如此反复多次实验,观察现象 | 试管中均产生大量气泡,带火星木条均复燃 |
③将实验②中的剩余物小心过滤,并将所得滤渣进行洗涤、干燥、称量,所得固体质量仍为ag | |
④分别量取5mL15%过氧化氢溶液放入C、D两支试管中,向C试管中加入ag氧化铁粉末,向D试管中加入ag二氧化锰粉末,观察现象 |
(1)A试管中反应的符号表达式为_________;B试管中的现象________。
(2)实验②、③证明:氧化铁的___________和____在反应前后均没有发生变化,可以作过氧化氢分解的催化剂;
(3)实验设计④的目的是_________,若实验![]() 观察到D试管中产生气泡的速率更快,由此你可以得到的结论是____。
观察到D试管中产生气泡的速率更快,由此你可以得到的结论是____。
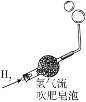
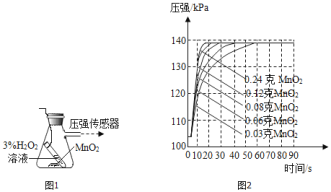
(4)兴趣小组同学设计了如图1实验装置,利用压强传感器测不同质量二氧化锰对双氧水分解快慢的影响。在8mL3%的双氧水中分别加入了0.03g,0.06g,0.08g,0.12g,0.24gMnO2测得容器内压强的变化曲线如图2所示![]() 曲线的斜率表征催化反应的速率
曲线的斜率表征催化反应的速率![]() 请观察如图,回答问题:
请观察如图,回答问题:
![]() Ⅰ
Ⅰ![]() 根据图2可发现:该实验条件下,30s内催化分解8mL浓度为
根据图2可发现:该实验条件下,30s内催化分解8mL浓度为![]() 的双氧水,MnO2的最小用量为_____g。
的双氧水,MnO2的最小用量为_____g。
![]() Ⅱ
Ⅱ![]() 根据图2,下列说法正确的是________。
根据图2,下列说法正确的是________。
a 二氧化锰用量越多,产生氧气越多
b 反应容器的气密性,对实验所测数据的精确度有影响
c 称量的二氧化锰质量的精确度对实验装置中最终的压强大小没有影响
(知识拓展)
若实验中ag氧化铁中a=0.25,则其中氧元素的质量为__________g。若经过精密仪器测得该氧化铁样品中铁元素和氧元素的质量比为21∶8,则该氧化铁样品中混有的另一物质是___________(填“FeO”或“Fe3O4”)