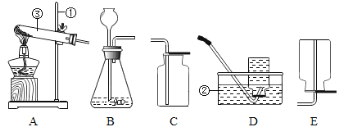
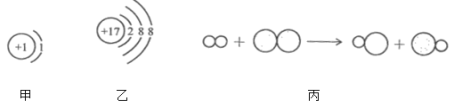【题目】重庆凤中的同学们在学习了催化剂的知识后提出:氧化铁固体(Fe2O3,难溶于水)在双氧水制氧气的反应中能否起到类似二氧化锰的催化作用呢?于是进行了以下探究:
(猜想)Ⅰ、Fe2O3既不是催化剂,也不是反应物,反应前后质量和化学性质不变;
Ⅱ、Fe2O3是反应物,要生成O2,反应前后质量和化学性质要改变;
Ⅲ、Fe2O3是该反应的催化剂,反应前后_____;
(实验)用天平称量1g Fe2O3固体,取10mL10%的双氧水于试管中,进行实验:

(1)实验过程中记录现象如下:
步骤①现象 | 步骤③现象 | 步骤⑥ | 结论 |
无明显变化 | _____ | 称得固体质量为1g | 猜想Ⅲ成立. |
(2)老师指出上述实验不能证明Fe2O3是该反应的催化剂,理由是_____(填序号);
A 只有二氧化锰能起催化作用
B 未验证回收的固体是否仍是Fe2O3
C 未验证回收的固体的物理性质
D 未验证Fe2O3是否改变反应速率
(3)步骤③中,试管中各物质质量随反应时间t变化曲线正确的是_____(填序号)。

【题目】研究和控制化学反应条件有重要意义。
(1)同学们想探究双氧水的浓度对反应速率的影响。在其他条件相同的情况下进行了三次实验,记录各收集一瓶相同体积氧气所需要的时间。
实验 | 30%双氧水的质量(g) | 加入的水的体积(mL) | 二氧化锰质量(g) | 收集时间(s) |
1 | 10 | 40 | 5 | 200 |
2 | 20 | 30 | 5 | 100 |
3 | 30 | 20 | 67 |
①写出上述反应的化学符号表达式_____。
②实验3中,加入的二氧化锰质量为_____g。
③相同条件下,实验3产生氧气的速率最快,说明_____。
(2)同学通过查阅资料得知,双氧水在70℃以上会较快分解产生氧气。为了验证加热双氧水也可以产生氧气,同学们进行实验。实验中观察到试管内产生气泡,但将带火星的木条放在导管口没有复燃,可能的原因是_____。
【题目】化学反应的程度与反应物的浓度之间有一定的规律可循。某实验小组各取等质量的木炭和等质量的硫分别在容积相同的集气瓶中燃烧。记录如下:
实验 | 实验步骤 | 实验现象 | 燃烧反应的化学符号表达式 | |
A | ①木炭在空气中燃烧 | ①木炭红热 | 产生的气体都能使澄清石灰水变浑浊 | _____ |
②木炭在氧气中燃烧 | ②_____ | |||
B | ③硫在空气中燃烧 | ③_____ | 产生的气体都有刺激性气味 | _____ |
④硫在氧气中燃烧 | ④明亮的蓝紫色火焰 | |||
通过A、B两组对比实验的现象,可以得出的规律是:_____。