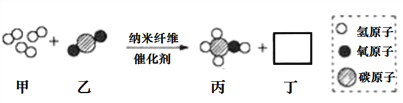
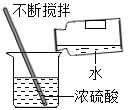
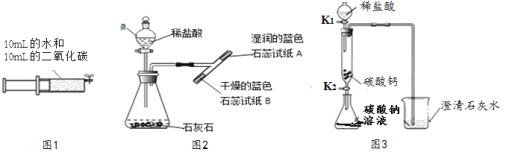
【题目】化学与生活息息相关。

(1)用过的铁锅保护不当很容易生锈,铁生锈的实质是铁与____发生复杂的化学变化,铁锈的主要成分是____。生活中防止铁锅生锈的一种方法____。
(2)“豌豆黄”是一道传统小吃:
品名 | 豌豆黄 |
主要原料 | 豌豆 |
主要营养成分 | 蛋白质、糖类、钠、钙、钾、镁等元素 |
“豌豆黄”中主要含有蛋白质、____和____等三类营养素,其中属于有机物的有____种。
(3)下列做法会造成水体污染的有____(填字母序号,下同)
A 工业废水直接排放 B 生活污水集中处理后排放
C 不使用含磷洗衣粉 D 大量使用化肥农药
(4)酒精和二甲醚(CH3OCH3)都可以可作为替代汽油、柴油的燃料,酒精完全燃烧的化学方程式为____;等质量的酒精和二甲醚在空气中完全燃烧产生水的质量比为____。
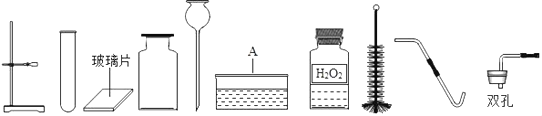
(5)实验室配制溶质质量分数为5%的氯化钠溶液,有以下操作:①溶解 ②称量 ③计算 ④装瓶贴标签。正确的顺序是____(填序号)。溶解操作中需要的仪器有____、____。量取蒸馏水时,若仰视读数,则导致溶质质量分数____(填“<”或“>”)5%。医院输液常用到的生理盐水是0.9%的氯化钠溶液。若用该氯化钠溶液加水稀释配制500毫升(密度约为1g/mL)生理盐水,需要5%的氯化钠溶液____克。
(6)生石灰与水反应后生成一种具有消毒能力的物质,该物质的化学式是____;“84消毒液”常用于公共场所杀菌消毒。测得稀释后的消毒液pH=9,实验室测定该数据可选用____(选填字母序号)。根据测定,该消毒液呈____性。
A 紫色石蕊 B pH试纸 C 无色酚酞 D 红色石蕊试纸
【题目】碳酸镁水合物是制备镁产品的中间体。
(制取MgCO3·3H2O)工业上从弱碱性卤水(主要成分为MgCl2)中获取MgCO3·3H2O的方法如下:
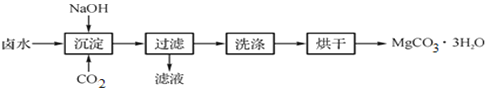
图1 获取MgCO3·3H2O的工艺流程
(1)沉淀过程的化学方程式为:MgCl2+CO2+2NaOH+2H2O![]() MgCO3·3H2O↓+2____。
MgCO3·3H2O↓+2____。
(2)沉淀过程的pH随时间的变化如图2所示,沉淀过程的操作为____(填字母)。
A 向卤水中滴加NaOH溶液,同时通入CO2
B 向NaOH溶液中滴加卤水,同时通入CO2
C 向卤水中通入CO2至饱和,然后滴加NaOH溶液,同时继续通入CO2
D 向NaOH溶液中通入CO2至饱和,然后滴加卤水,同时继续通入CO2
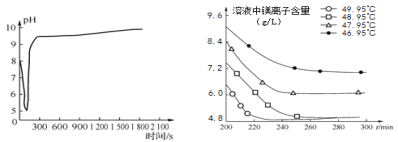
图2 沉淀过程的pH变化 图3 不同温度下溶液中镁离子含量随时间的变化
表1 不同反应温度下的水合碳酸镁
温度(℃) | 产物 |
46.95 | MgCO3·3H2O |
47.95 | MgCO3·3H2O |
48.95 | MgCO3·3H2O |
49.95 | Mg5(OH)2(CO3)4·4H2O |
(3)沉淀过程的溶液中镁离子含量随时间的变化如图3所示,不同温度下所得到沉淀产物如表1所示。则沉淀过程选择的温度为____,理由是____。
(测定MgCO3·3H2O的纯度)
利用下图所示装置(图中夹持仪器略去)进行实验,以确定MgCO3·3H2O的纯度。
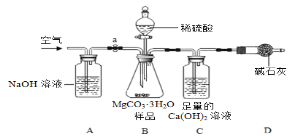
依据实验过程回答下列问题:
(1)实验过程中需持续____(选填“缓缓”或“迅速”)通入空气,其作用除了可搅拌B、C中的反应物外,还有____。D中碱石灰的作用为____。
(2)下列各项措施中,不能提高测定准确度的是____(填标号)。
A 在加入硫酸之前,应排净装置内的CO2气体
B 为了缩短实验时间,快速滴加硫酸
C 在A~B之间增添盛有浓硫酸的洗气装置
D 在C装置左侧导管末端增添多孔球泡
(3)实验中准确称取15.0 g样品三份,进行三次测定,测得中生成CaCO3沉淀的平均质量为10.0 g。请计算样品中MgCO3·3H2O的纯度________
(4)小明认为应将澄清石灰水换成Ba(OH)2溶液,其理由除了Ba(OH)2溶解度大,浓度大,使CO2被吸收的更完全外,还有____。
(5)若获取MgCO3·3H2O的样品中含有少量Mg5(OH)2(CO3)4·4H2O,则样中MgCO3·3H2O的纯度____(填“偏大”或“不变”或“偏小”)
【题目】硫酸亚铁铵晶体俗名为摩尔盐,在制药、电镀方面有广泛的应用。
资料: ①硫酸亚铁铵晶体化学式为FeSO4·(NH4)2SO4·6H2O,相对分子质量为392,易溶于水,不溶于乙醇;
②相关物质的溶解度(单位:g)如下表:
温度/℃ | FeSO4 | (NH4) 2SO4 | FeSO4·(NH4)2SO4·6H2O |
10 | 20.0 | 73 | 17.2 |
20 | 26.5 | 75.4 | 21.6 |
30 | 32.9 | 78 | 28.1 |
③硫酸亚铁铵晶体受热时,在200℃以下只有结晶水失去。
某兴趣小组的学生用含有少量铜的废铁屑制备硫酸亚铁铵晶体,流程如下:
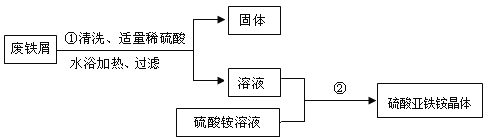
(1)操作①中发生反应的化学方程式为____;过滤所需玻璃仪器有烧杯、玻璃棒、____;
(2)操作①中过滤时,要趁热进行的原因是____;
(3)操作②的目的是得到硫酸亚铁铵晶体。操作顺序是b→ ____ → ____ →d;
a 过滤 b 加热浓缩 c 冷却结晶 d 洗涤干燥
(4)操作②中使用乙醇洗涤,这样做的优点是____;(选填字母序号)
A 避免用水洗涤所造成的晶体损耗 B 酒精易挥发,可低温晾干晶体
(5)该实验取废铁屑15 g,最终得到硫酸亚铁铵晶体39.2 g,则原废铁屑中铁元素的质量分数不低于____(精确到0.1%,不要求写过程)。