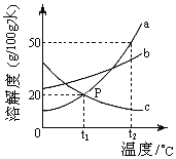
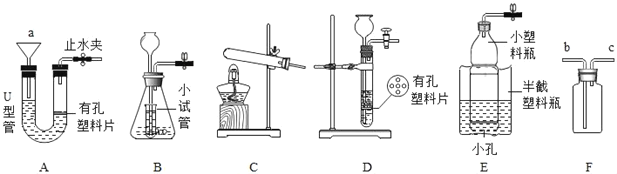
【题目】同学们做甲、乙两个盐跟盐反应的分组实验(见图)。

(1)甲组实验中观察到的现象是___。
(2)乙组实验中反应的化学方程式为___。
(3)实验结束后,甲、乙两组同学将全部的浊液集中倒进一个废液缸中(如图丙)。丙组同学对浊液进行过滤,探究滤液的成分。
(提出问题)滤液里除了NaCl外,还有什么物质?
(提出猜想)猜想Ⅰ:___;猜想Ⅱ:Na2SO4;猜想Ⅲ:Na2CO3;猜想Ⅳ:Na2CO3和Na2SO4
(实验探究)
探究方案 | 实验现象与结论 |
①若现象a只有白色沉淀,则猜想__成立。 ②若现象a只有__,则猜想Ⅲ和猜想Ⅳ可能成立。 | |
当现象b产生白色沉淀时,再向白色沉淀加入稀硝酸, ③若沉淀全部不溶解且无气泡产生,则猜想__成立; ④若沉淀全部溶解且__,则猜想Ⅲ成立; ⑤__且产生气泡,则猜想Ⅳ成立。 |
(拓展与思考)上述滤液的成分不可能出现的组合是BaCl2、Na2CO3和Na2SO4,原因是___。

【题目】废铁屑的主要成份是铁,同时还有少量铁锈(Fe2O3),如图是动物饲料硫酸亚铁的生产工艺:

查阅资料:+2价的铁元素容易被空气中的氧气氧化。
回答下列问题:
(1)在反应器中发生反应的化学方程式除Fe2(SO4)3+Fe=3FeSO4外,还有__、__。
(2)操作A所用到的玻璃仪器有漏斗、玻璃棒和__。
(3)滤液M中肯定含有的溶质的化学式是__(只写一种)。
(4)已知硫酸亚铁的溶解度和析出晶体的组成如下表
温度/℃ | 0 | 10 | 30 | 40 | 50 | 60 | 64 | 70 | 80 | 90 |
溶解度/g | 15.6 | 20.5 | 33.0 | 40.4 | 48.8 | 55.0 | 55.3 | 50.6 | 43.7 | 37.2 |
析出晶体 | FeSO47H2O | FeSO44H2O | FeSO4H2O | |||||||
根据上表,硫酸亚铁晶体(FeSO47H2O)冷却结晶温度最高不超过__℃.则操作B的步骤是:将滤液M在氮气环境中__、冷却结晶、过滤,即可得晶体,其中氮气的作用是__。