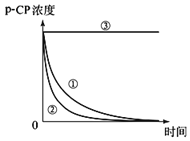
【题目】Fenton法常用于处理含难降解有机物的工业废水。其原理是利用Fe2+和H2O2反应产生能降解污染物的活性成分。现运用该方法降解有机污染物p-CP,探究有关因素对降解反应速率的影响。实验时,p-CP的初始浓度相同,温度恒为25℃或40℃.实验测得p-CP的浓度随时间变化的关系如图。
请回答
(1)请完成以下实验设计表。
实验 编号 | 实验目的 | 温度/℃ | pH | 浓度/(mgL-1) | |
H2O2 | Fe2+ | ||||
① | 为②③提供参照 | 25 | 3 | 204 | 16.8 |
② | 探究温度对降解反应速率的影响 | ______ | 3 | 204 | 16.8 |
③ | 探究溶液pH对降解反应速率的影响 | 25 | 10 | 204 | 16.8 |
(2)实验①、②表明温度升高,降解反应速率______。
(3)进一步实验发现,温度过高时,降解反应较难发生。请从所用试剂H2O2的角度分析原因:______。
(4)为测定不同时间内有机物降解的浓度,需在不同时间从反应器中取样,并使所取样品中的降解反应立即停止。根据图示信息,请写出迅速停止反应的一种方法:______。
【题目】用已知溶质质量分数的溶液可以测定未知溶液的溶质质量分数。实验室有一瓶标签模糊的稀盐酸,某同学为了测定其溶质质量分数,进行了如下实验:
①取一洁净的锥形瓶称量,然后往其中加入一定量的稀盐酸,并滴入几滴紫色石蕊试液(质量忽略不计),重新称量。
②往上述锥形瓶中逐滴加入溶质质量分数为 16%的氢氧化钠溶液,边滴加边振荡,当观察到溶液由红色恰好变为紫色时,停止滴加,再次称量。数据如下表:
锥形瓶 | 锥形瓶+稀盐酸 | 锥形瓶+反应后溶液 | |
质量/克 | 35.5 | 55.5 | 80.5 |
(1)实验中消耗的氢氧化钠溶液质量为______克。
(2)反应后溶液中的溶质质量分数是多少______?
(3)另有同学做了同样的实验,却得到不同的结果。用精密pH试纸测得反应后锥形瓶内溶液的pH为7.8,则他测出的盐酸溶质质量分数偏大还是偏小,造成偏差的原因是______。
【题目】碳酸钠广泛用于造纸、纺织、制革等工业,是一种重要的化工原料。我国侯德榜发明了将制碱与制氨结合起来的联合制碱法,为碳酸钠的工业化生产作出了巨大贡献。
(查阅资料)侯氏制碱法中主要反应:
Ⅰ.NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl
Ⅱ.2NaHCO3=Na2CO3+H2O+CO2↑
(实验探究)小明以粗盐配制饱和食盐水,并采用如图1所示装置模拟制备碳酸氢钠,进而制得碳酸钠。

实验操作如下:
①关闭K1,打开K2通入NH3,调节气流速率,待其稳定后,打开K1通入CO2;
②待三颈烧瓶内出现较多固体时,关闭K2停止通NH3,一段时间后,关闭K1停止通CO2;
③将三颈烧瓶内的反应混合物过滤、洗涤、低温干燥,并将所得固体置于敞口容器中加热,记录剩余固体质量。请回答下列问题:
加热时间/min | t0 | t1 | t2 | t3 | t4 | t5 |
剩余固体质量/g | 未记录 | 15.3 | 13.7 | 11.9 | 10.6 | 10.6 |
(1)粗盐中除了含有泥沙等不溶性杂质,还含有少量的MgCl2等。若要除去粗盐中的MgCl2,可加入过量的NaOH溶液,写出对应的化学方程式______,再过滤,然后向滤液中加入适量______,得到氯化钠溶液。
(2)饱和NaHCO3溶液的作用是除去CO2中混有的HCl,反应的化学方程式为______。
(3)三颈烧瓶上连接的长颈漏斗的主要作用是______,有同学认为应该在长颈漏斗内放置一团蘸有酸液的棉花,理由是______;关闭K2停止通NH3后,还要继续通一段时间CO2,其目的是______。
(4)根据实验记录,计算t2时NaHCO3固体的分解率(已分解的NaHCO3质量与加热前原NaHCO3质量的比值),请写出计算过程_____。
(拓展延伸)小华设计如图2的实验装置测定某纯碱样品(含少量杂质NaCl)中碳酸钠的质量分数:取一定量的样品与足量稀硫酸反应,通过排饱和碳酸氢钠溶液测定生成CO2的体积,计算样品中碳酸钠的质量分数。(已知常温常压下CO2的密度是1.977g/L)
(1)如果样品质量为5.3g,则实验中选用的量气管规格最合适的是______(填字母)。
A.500mLB.1000mLC.1500mLD.2000mL
(2)若实验中测得碳酸钠质量分数偏小,下列可能的原因是______。
a.装置漏气
b.读取数据时量气管的液面低于水准管的液面
c.反应结束后烧瓶中有CO2残留
d.读取数据时仰视读数
e.稀硫酸加入烧瓶占据体积
【题目】草酸镍晶体(NiC2O42H2O)可用于制镍催化剂。某小组用废镍催化剂(成分为Fe2O3、Ni、Fe、SiO2等)制备草酸镍晶体的部分实验流程如图所示:
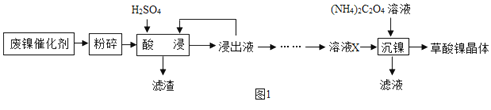
已知:①Ni能和稀H2SO4反应。
②相关金属离子生成氢氧化物沉淀的pH如下表
金属离子 | 开始沉淀的pH | 完全沉淀的pH |
Fe3+ | 1.1 | 3.2 |
Fe2+ | 5.8 | 8.8 |
Ni2+ | 6.7 | 9.5 |
③H2O2能将Fe2+氧化为Fe3+
(1)废镍催化剂“粉碎”的目的是______。
(2)保持其他条件相同,在不同温度下对废镍催化剂进行“酸浸”,镍浸出率随时间变化如图,“酸浸”的适宜温度与时间分别为______(填字母)。
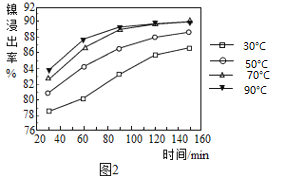
A 30℃、30min B 90℃、150min C 70℃、120min D 90℃、120min
(3)“酸浸”中发生的反应方程式为______(写1个即可)。
(4)“浸出液”得到“溶液x”过程中,加入试剂先后顺序是______(填字母)
A.先加H2O2溶液,再加NaOH溶液 B.先加NaOH溶液,再加H2O2溶液加NaOH溶液调节pH______(填范围),充分反应后得到滤渣的操作是______,该操作中所用到的玻璃仪器有玻璃棒、烧杯和______,其中玻璃棒的作用是______。
(5)将“沉镍”工序:①主要过程为:蒸发浓缩、______、过滤,所得固体用75%乙醇洗涤、110℃下烘干,得草酸镍晶体。
②用75%乙醇洗涤的目的是洗去杂质、______。
③烘干温度不超过110℃的原因是______。