【题目】某化学兴趣小组为测定一批石灰石样品中碳酸钙的质量分数,取10g石灰石样品,把40g稀盐酸分4次加入样品中(样品中的其它成分既不与盐酸反应,也不溶于水),充分反应后经过滤、干燥、称量等操作,实验数据如下表:
实验 | 第一次 | 第二次 | 第三次 | 第四次 |
稀盐酸的用量 | 10g | 10 g | 10 g | 10 g |
剩余固体的质量 | X g | 4 g | 2 g | 2 g |
(1)表中X的值 为________g;
(2)该石灰石样品中碳酸钙的质量分数为_______;
(3)计算实验过程中产生二氧化碳气体的质量_______。(写出计算过程)
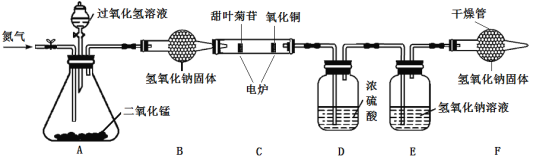
【题目】某化学活动兴趣小组用如图装置进行一氧化碳还原氧化铜的探究实验,反应一段时间后,玻璃管内黑色粉末全部变成红色,澄清石灰水变浑浊。
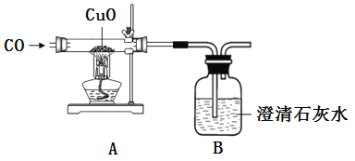
(1)从安全环保的角度考虑,上述实验需要改进的是______。
(2)装置A中发生反应的化学方程式为_____。
(3)同学们通过查阅资料得知:①氧化亚铜(Cu2O)和铜均为红色固体;②铜不与稀硫酸反应,Cu2O能和稀硫酸反应(化学方程式为Cu2O+H2SO4=CuSO4+Cu+H2O);③硫酸铜溶液为蓝色。他们对反应后玻璃管中的红色固体进行如下探究:
(提出问题)反应后生成的红色固体成分是什么?
(作出猜想)猜想一:红色固体只有Cu
猜想二:红色固体只有Cu2O
猜想三:红色固体为______。
(实验探究)设计如下实验方案
实验操作 | 现象 | 结论 |
甲同学取少量红色固体于试管中, 加入过量的稀硫酸。 | _________ | 猜想一正确。 |
乙同学另取少量红色固体于试管中,加入过量的稀硫酸。 | 溶液变蓝色,有红色固体剩余。 | 猜想二正确。 |
(思考与分析)乙同学认为猜想二正确,同学们分析后认为他的结论不准确,理由是________。为此,同学们补充进行了以下实验:称取mg红色固体于试管中,加入过量的稀硫酸充分反应,然后过滤、洗涤、干燥、称量,得到ng固体。当n>______(含m的代数式)时,可以得出猜想三的结论正确。