【题目】如下图是某品牌陈醋的部分标签。

(1)原料“糯米、大米”的主要成分都是___________;
A.碳水化合物 B.油油脂 C.蛋白质
(2)原料中的食盐由构成____________;
A.分子 B.原子 C.离子
(3)用陈醋在铁锅中烹任糖醋排骨时,写出醋酸(HAc)与铁发生反应的化学方程式:___________
(4)已知食醋的等级按下表划分,这瓶陈醋的等级_____________(填:特级、优级、一级、二级)
等级 | 特级 | 优级 | 一级 | 二级 |
总酸g/100mL | ≥6.00 | 5.50~5.99 | 5.00~5.49 | 4.50~4.99 |
(5)请根据所学知识再补充一个该陈醋的贮存条件___________________________________。
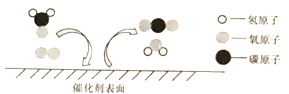
【题目】用甲和乙反应制备燃料丙。根据下列微观示意图得出的结论中,正确的是

A. 甲的化学式为CH2 B. 反应中甲、乙、丙的分子个数比为2:1:1
C. 甲、乙、丙都是氧化物 D. 乙中氢元素质量分数最低
【题目】电池是日常必备用品之一,但它也是环境污染的一个重要来源。下面是某兴趣小组利用废旧锌锰干电池作为原料,并进行相关探究的过程。
(知识储备)(1)锌锰电池的构造和组成(见图)。
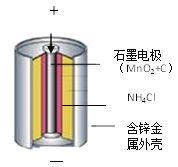
(2)结晶水合物的特殊性质:在逐步升高温度条件下,结晶水合物能失去部分或者全部结晶水,如蓝色的胆矾晶体(CuSO4 5H2O)受热时可失去结晶水变为白色的无水硫酸铜粉末(CuSO4)。
I.制备皓矾晶体(ZnSO4xH2O)
小组同学参观了某回收废旧锌锰电池的工厂,其回收工艺流程如图:

⑴流程图中试剂a的化学式是__________;得到的滤液1农业上可用作_____________。
(2)将滤渣B在空气中充分灼烧 可提纯制得的固体是___________,该方法提纯的原理是(用化学方程式回答)____________________________。
⑶将滤液2中溶质主要是硫酸锌,其有关溶解度和温度关系如下表,
温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
溶解度/g | 41.8 | 54.1 | 70.4 | 74.8 | 67.2 | 60.5 |
将滤液2蒸发浓缩、__________,可得到皓矾晶体(ZnSO4xH2O)。
II.皓矾晶体中结晶水含量的测定
小组同学将部分皓矾晶体(ZnSO4xH2O)带回实验室,用下图装置测定晶体中结晶水的含量(图中半透膜可让气体通过又可防止固体粉末进入导管)。

测定方法:称取28.7g晶体置于C装置的硬质玻璃管中,加热至完全失去结晶水:(ZnSO4xH2O == ZnSO4 + xH2O),冷却至常温后,称量玻璃管中固体其质量为16.1g。
⑷A中的化学方程式是_____________,B中的试剂可从下列物质中选取,你的选择是__________________。
A.浓硫酸 B.硝酸银溶液 C.饱和碳酸钠溶液 D.澄清石灰水
⑸实验过程中若不通入CO2测得的结果将________(填“偏大”、 “偏小”或“无影响”)。
根据实验结果,计算皓矾晶体中结晶水的x值。计算过程:__________________
⑹将上述皓矾晶体加热会逐渐失去部分结晶水,加热过程中有关残留固体质量如下图,写出D-E段发生反应的化学方程式________________