【题目】为了测定黄铜(铜、锌合金)中铜的质量分数,取黄铜样品20g加入大烧杯中,把200g稀盐酸分四次加入,实验所得数据如表:
实验次数 | 第1次 | 第2次 | 第3次 | 第4次 |
加入稀盐酸的质量/g | 50 | 50 | 50 | 50 |
剩余固体的质量/g | 16.75 | 13.5 | m | 12.2 |
分析表中数据,完成下列问题:
(1)表中m=______;
(2)反应总共产生气体的质量为多少?(写出计算过程)
(3)若200g稀盐酸中HCl的质量为14.6g,其余都为水.反应结束后大烧杯中氢元素的质量为______g.
【题目】金属用途广泛,其结构和性质等是化学的重要研究内容。
(1)下图是铝的原子结构示意图。下列说法不正确的是 。
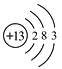
A.铝原子的质子数为13 |
B.在化合物中铝通常显+3价 |
C.铝是地壳中含量最多的元素 |
D.铝可作导线是由于它具有良好的导电性 |
(2)某化学小组用一定量AgNO3和Cu(NO3)2混合溶液进行了下图实验,并对溶液A和固体B的成分进行了分析和实验探究。

【提出问题】溶液A中的溶质可能有哪些?
【作出猜想】①只有Zn(NO3)2② Zn (NO3)2、AgNO3③ Zn (NO3)2、Cu(NO3)2④Zn (NO3)2、AgNO3、Cu(NO3)2
【交流讨论】不合理的猜想是 (填标号),其理由是 。
【实验探究】若猜想①成立,通过以下实验可确定固体B的成分,请将下表填写完整。
实验步骤 | 现 象 | 有关反应的化学方程式 |
取少量固体B, | 有气泡产生 |
|




