【题目】某化学兴趣小组的同学对一包久置的生石灰(化学式为CaO)干燥剂产生了好奇,于是他们对这包干燥剂的成分展开了探究。
【资 料】生石灰与水发生的反应属于放热反应
【提出问题】这包干燥剂是否变质,成分是什么?
【猜想假设】
猜想一:全部是CaO;猜想二:是CaO和Ca(OH)2的混合物;猜想三:全部是Ca(OH)2;猜想四:是Ca(OH)2和CaCO3的混合物。
【实验探究】
(1)取部分该干燥剂于试管中,加水后无放热现象,说明这包干燥剂中不含________。
(2)继续向试管中滴加足量稀盐酸,有气泡出现,说明这包干燥剂中含有__________。
(3)为了进一步确定这包干燥剂中有无其他成分,小组同学设计了以下两种方案。
另取部分干燥剂于烧杯中,加水并搅拌,静置后取上层清液于2支试管中,请你参与实验并完成表中空白。
实验方案 | 方案一 | 方案二 |
实验操作 |
|
|
实验现象 | 溶液由无色变为红色,则溶液的PH______7 (填“﹤”“﹥” 或“﹦”) | 澄清溶液变浑浊 |
写出方案二发生的化学反应方程式_______________________________。
【实验结论】通过以上实验探究,得出猜想___________成立。
【题目】化学兴趣小组的同学对“影响金属与盐酸反应的剧烈程度的因素”进行了探究。
【提出问题】金属与盐酸反应剧烈程度受哪些因素的影响?
【作出猜想】a.可能与金属本身的性质有关
b.可能与盐酸的浓度有关
【设计探究】为保证实验准确性,实验所用金属片均用砂纸打磨,打磨目的主要是:______________________________。
实验⑴为探究猜想a,小组同学分别在两支试管中放入相同质量的锌片和铁片,然后分别加入等质量、等浓度的稀盐酸,观察到放锌片的试管中立即产生大量气泡,放铁片的试管中只产生少量气泡。写出锌与盐酸发生反应的化学方程式为_____________________________。
从实验现象可判断:金属活动性Zn_______Fe(填“<”、“=”或“>”)。
【得出结论1】
金属与盐酸发生反应的剧烈程度与金属本身性质有关,金属的活动性与反应的剧烈程度的关系是_____________________________________________________。
实验⑵为探究猜想b,小组同学设计如图的装置进行实验,其中注射器的作用是__________。
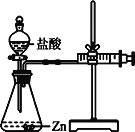
所用药品、实验数据如下表:
实验 编号 | 选用金属 (均取2g) | 盐酸质量分数 (均取50mL) | 每分钟产生氢气的体积/mL | |||||
1分钟 | 1﹣2 分钟 | 2﹣3 分钟 | 3﹣4 分钟 | 4﹣5 分钟 | 前5分 钟共收 集气体 | |||
Ⅰ | 锌片 | 15% | 2.9 | 16.9 | 11.9 | 9.2 | 7.6 | 48.5 |
Ⅱ | 锌片 | 5% | 1.6 | 8.4 | 5.9 | 4.8 | 3.7 | 24.4 |
【得出结论2】金属与盐酸发生反应的剧烈程度与盐酸的浓度有关,其关系是________________。
[注意:若答对下面小题奖励4分,化学试卷总分不超过60分]
【反思评价】根据表中实验Ⅱ数据分析,请解释锌与盐酸发生反应由慢到快原因:_________________再由快到慢的原因是_________________。
【拓展延伸】通过以上探究,你认为金属与盐酸反应的剧烈程度还可能与哪些因素有关?
因素1:_______________________________。
因素2:_______________________________。