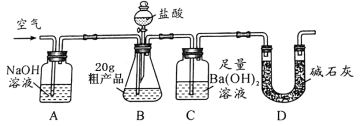
【题目】下列四个图像中,能正确反映对应变化关系的是
|
|
|
|
A.将水通电一段时间 | B.向一定量的氢氧化钠溶液中逐滴加入pH = 2的稀盐酸至过量 | C.向两份完全相同的稀盐酸中分别加入锌粉、镁粉 | D.某温度时,向一定量的饱和石灰水中加入少量生石灰 |
【题目】(7分)一次趣味化学活动中,王老师向同学们展示了一瓶标签受损的无色溶液,如下图所示。
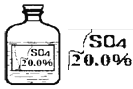
要求同学们进行探究:
确认这瓶溶液到底是什么溶液?
提出猜想:王老师提示:这瓶无色溶液只能是以下四种溶液中的一种:
①硫酸镁溶液、 ②硫酸钠溶液、
③硫酸溶液、 ④硫酸铵溶液。
查阅资料:
A:常温下,相关物质的溶解度如下
物质 | MgSO4 | Na2SO4 | (NH4)2SO4 | H2SO4 |
溶解度 | 35.1g | 19.5g | 75.4g | 与水任意比互溶 |
B:(NH4)2SO4的水溶液显酸性
【实验探究】
(1)通过查阅资料,小明同学认为猜想 (填序号)不成立,原因是 。
(2)为确定其它几种猜想是否正确,小明同学继续进行探究:
实验步骤 | 实验现象 | 实验结论 |
a取该溶液少许于试管中,向其中滴加几滴氢氧化钠溶液 | 溶液中有白色沉淀生成 | 猜想①成立 |
b取该溶液少许于试管中,向其中滴加几滴紫色石蕊溶液 | 猜想③成立 |
小芳同学认为小明实验步骤b的结论不正确,她的理由是 ;
(3)请你设计实验方案,确认该溶液是硫酸铵溶液并完成实验报告:
实验操作 | 实验现象 | 实验结论 |
取该溶液少许于试管中,再往该溶液加入 溶液,加热。 | 猜想④成立,该反应的化学方程式为 |