0 181933 181941 181947 181951 181957 181959 181963 181969 181971 181977 181983 181987 181989 181993 181999 182001 182007 182011 182013 182017 182019 182023 182025 182027 182028 182029 182031 182032 182033 182035 182037 182041 182043 182047 182049 182053 182059 182061 182067 182071 182073 182077 182083 182089 182091 182097 182101 182103 182109 182113 182119 182127 211419
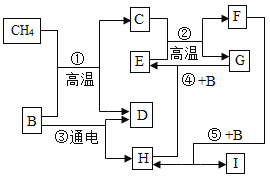
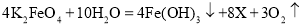 。 x的化学式为_____________________;
。 x的化学式为_____________________;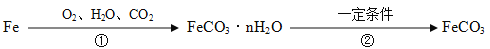
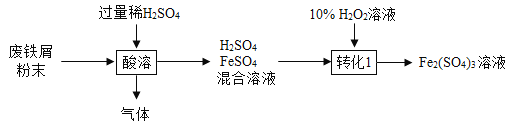
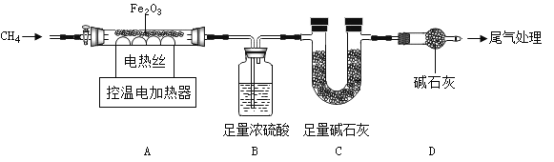
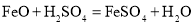
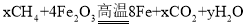 。下列说法正确的是_____________________;(选填序号)。
。下列说法正确的是_____________________;(选填序号)。 点燃酒精灯 B.
点燃酒精灯 B. 取用固体药品
取用固体药品 加热液体 D.
加热液体 D.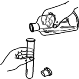 倾倒液体
倾倒液体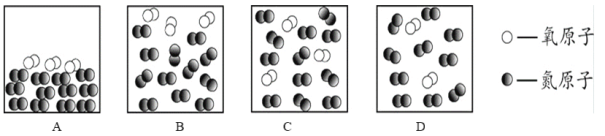
 Na2SiO3+X+H2O,下列有关X物质的化学式推断中,正确的是( )
Na2SiO3+X+H2O,下列有关X物质的化学式推断中,正确的是( )