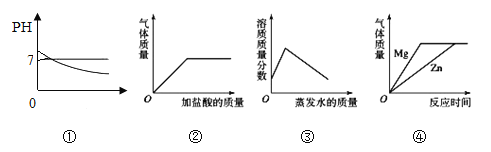
某同学对下列四个实验都设计了两种方案,其中两种方案都合理的是()
选项 | 实验目的 | 方案1 | 方案2 |
A | 鉴别稀硫酸与稀盐酸 | 加BaCl2溶液 | 加紫色石蕊试液 |
B | 鉴别(NH4)2SO4与K2SO4 | 熟石灰、研磨、嗅气味 | 加水观察是否溶解 |
C | 除去铜粉中的少量铁粉 | 加过量稀硫酸溶液、过滤 | 用磁铁吸引 |
D | 清洗衣服上的铁锈 | 稀盐酸洗 | 汽油洗 |
A.A B.B C.C D.D
X、Y、Z、W是四种不同的金属,为比较金属活动性的强弱,某同学利用这四种金属单质、盐酸、Z的硝酸盐、W的硝酸盐,进行有关实验,结果如下表(能发生置换反应的记为“√”,不能反应的记为“一”,无标记的表示未做该实验)。这四种金属的活动性顺序为 ( )
X | Y | Z | W | |
盐酸 | √ | — | — | √ |
Z的硝酸盐 | √ | |||
W的硝酸盐 | √ | — |
A.X>W>Y>Z B.X>Y>W>Z C.W>X>Y>Z D.Y>W>Z>X
已知复分解反应2CH3COOH+Na2CO3=2CH3COONa+H2O+CO2↑可进行。在常温下,测得相同浓度的下列六种溶液的pH:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
pH | 8.8 | 8.6 | 11.6 | 10.3 | 11.1 |
表中数据揭示出复分解反应的一条规律,即碱性较强的物质发生类似反应可以生成碱性弱的物质。依照该规律,请你判断下列反应不能成立的是
A. CO2+H2O+2NaClO=Na2CO3+2HClO B. CO2+H2O+NaClO=NaHCO3+HClO
C. CH3COOH+NaCN=CH3COONa+HCN D. NaClO+CH3COOH=HClO+CH3COONa
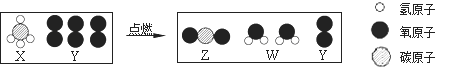
 CO2+H2O
CO2+H2O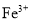 而带黄色,若某工业品盐酸中
而带黄色,若某工业品盐酸中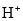 和
和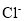 的个数比为91∶94,则该盐酸中
的个数比为91∶94,则该盐酸中