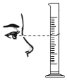
某组同学将碳酸钠溶液和一瓶标签破损的溶液M(如图)进行反应,有白色沉淀产生,过滤后得到澄清滤液。同学们对该实验进行了一系列的探究。
(提出问题)M溶液中的溶质是什么?
①是Ca(OH)2 ②是CaCl2
(收集资料)CaCl2水溶液呈中性
(设计实验)同学们设计了如下方案并进行实验:
实验操作 | 实验现象 | 实验结论 |
取少量M溶液于试管中,向其中滴入_____; | 溶液变红 | M是Ca(OH)2 |
(提出猜想)过滤后澄清滤液中含有哪些溶质
猜想一:NaOH;
猜想二:NaOH和_____;
猜想三:NaOH和Na2CO3。
(实验验证)同学们针对“猜想三”进行如下实验:
实验操作 | 实验现象 | 实验结论 |
取滤液于试管中,缓缓滴入几滴稀盐酸 | 没有气泡产生 | “猜想三”不成立 |
他们对实验结论的判断_____(填“正确”或“不正确”)。
(继续探究)设计如下实验方案确定滤液中溶质的组成:
实验操作 | 实验现象 | 实验结论 |
分别取少量滤液于A、B两支试管中, 在A试管中加入CaCl2溶液, 在B试管中加入Na2CO3 溶液。 | 若A中产生白色沉淀,B中没有沉淀 | “猜想三”成立 |
若A中没有沉淀,B中的现象 是_____; | “猜想二”成立 | |
若A、B中都没有沉淀产生 | “猜想一”成立 |
(反思与拓展)当反应后溶液中溶质只有NaOH时说明反应物之间量的关系是_____。
为测定某地石灰石中碳酸钙的质量分数,某兴趣小组将一定质量的石灰石样品粉碎后分成两等份,进行如下实验:
(1)一份放于烧杯中,向烧杯中逐渐加入某一浓度的盐酸,反应过程测得剩余固体质量与加入盐酸的质量关系如图1所示(石灰石中的杂质不与盐酸反应,也不溶与水)。请回答下列问题:
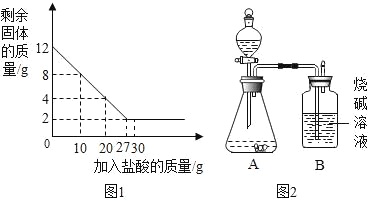
①石灰石样品中碳酸钙的质量分数_____;
②通过计算求所用盐酸的溶质质量分数。_____
(2)另一份进行如图2所示的实验:把产生的CO2气体用足量的烧碱溶液吸收,同时测量B瓶烧碱溶液增加的质量,结果如下表所示:
时间/分 | 0 | 1 | 2 | 3 | 4 | 5 | 6 |
B增加的质量 | 0 | 2 | 3 | 4 | 4.6 | X | 4.6 |
①上表中,第5分钟时,x=_____;
②该实验测得样品中碳酸钙的质量分数_____(填大于、小于或等于)另一实验,其原因可能是_____。
 钻石 B.
钻石 B.  涤纶衬衫
涤纶衬衫 青花瓷盘 D.
青花瓷盘 D.  金碗
金碗
 B.
B. 
 D.
D. 
 Fe3O4
Fe3O4