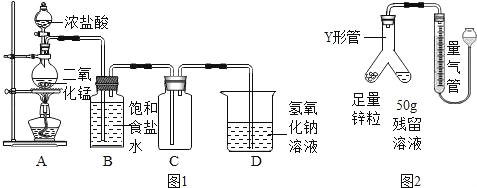
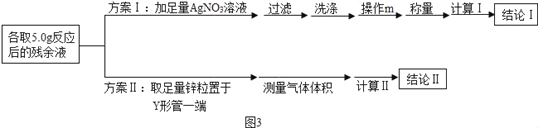
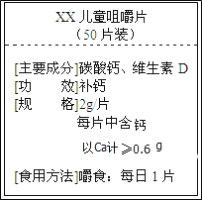
下列根据实验目的所设计的实验方案正确的是( )
选项 | 实验目的 | 实验设计 |
A | 除去CO2中的CO | 点燃 |
B | 测定某地雨水是否为酸雨 | 加紫色石蕊,观察颜色变化 |
C | 检验氢氧化钠溶液是否变质 | 加无色酚酞,观察颜色变化 |
D | 探究燃烧的条件之一是需要可燃物 | 用棉花分别蘸酒精和水,放在酒精灯火焰上加热片刻,观察现象 |
A. A B. B C. C D. D
小明同学家新换了水龙头,从说明书上了解到该水龙头是钢质镀铬。好奇的小明想探究铬(Cr)与常见金属铁、铜的活动性强弱,遨请你一同参加。
(1)作出猜想:
猜想1:Cr>Fe>Cu
猜想2:Fe>Cu>Cr
猜想3:你的猜想是___。
[查阅资料]
①铬是银白色有光泽的金属,在空气中其表面能生成抗腐蚀的致密的氧化膜。
②铬能与稀硫酸反应,生成蓝色的硫酸亚铬(CrSO4)溶液。
(2)设计实验
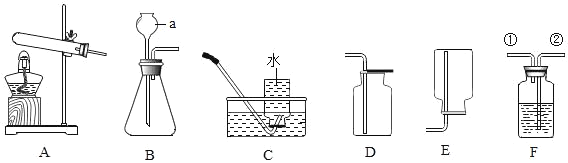
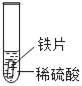
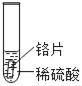
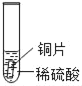
小明同学取大小相等的三种金属片,用砂纸打磨光亮;再取三支试管,分别放入等量的同种稀硫酸。
实验 | 试管1 | 试管2 | 试管3 |
实验操作 |
|
|
|
实验现象 | 铁片表面产生气泡较慢,溶液变为浅绿色 | 铬片表面产生气泡较快,溶液变成为蓝色 | ___ |
(3)结论与解释:
①小明得到的结论是猜想___正确。
②实验前用砂纸打磨金属片的目的是___。
(4)反思:小明将铬片投入FeSO4溶液中,现象是___,请你写出反应的化学方程式___。
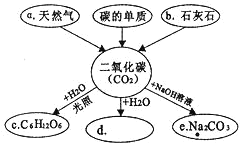
 MnCl2+Cl2↑+2H2O.
MnCl2+Cl2↑+2H2O.