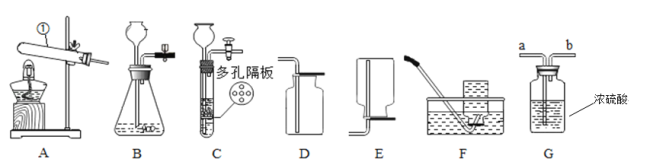
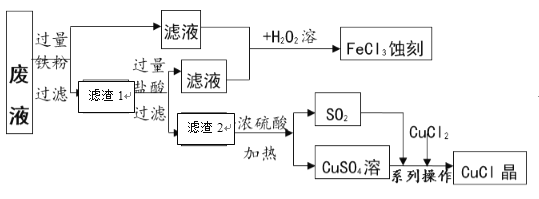
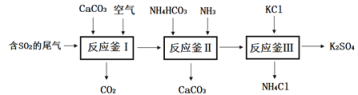
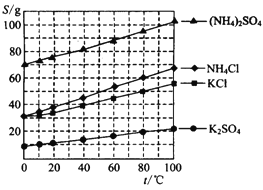
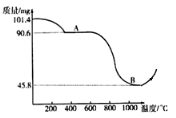
实验是学习化学中的重要手段,以下实验方法和操作中不能达到实验目的的是
选项 | 实验目的 | 实验方法和操作 |
A | 鉴别O2和CO2 | 分别伸入燃着的木条 |
B | 鉴别NaOH、NaCl | 取样于表面皿中,观察固体是否潮解 |
C | 除去NaCl溶液中混有的CaCl2 | 加适量K2CO3溶液、过滤 |
D | 除去FeSO4溶液中的CuSO4 | 加足量Fe粉,过滤 |
A. A B. B C. C D. D
总结、归纳知识,有利于提升学习能力,下列知识归纳有错误的一组是
A、化学与生活 | B、化学与健康 |
①用盐酸除铁锈痕迹 ②用NaOH溶液清洗手上的油污 ③草木灰与铵态氮肥混合施用增加肥效 | ①人体缺钙会导致骨质疏松 ②霉变大米洗净烧熟后不可食用 ③人体缺乏维生素C会引起坏血病 |
C、化学与安全 | D、化学与发现 |
①存放易燃易爆物不能堆放过高过密 ②油锅着火可用锅盖盖灭 ③实验时不得尝药品的味道 | ①门捷列夫发现了元素周期表 ②拉瓦锡用实验证明了空气的组成 ③侯德榜发现了联合制碱法 |
A. A B. B C. C D. D
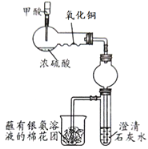
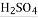 CO↑+H2O;银氨溶液能吸收CO气体。为探究??一氧化碳和氧化铜的反应原理,某校化学小组设计如图(加热仪器酒精灯略)实验,以下关于该实验的说法错误的是
CO↑+H2O;银氨溶液能吸收CO气体。为探究??一氧化碳和氧化铜的反应原理,某校化学小组设计如图(加热仪器酒精灯略)实验,以下关于该实验的说法错误的是