题目内容
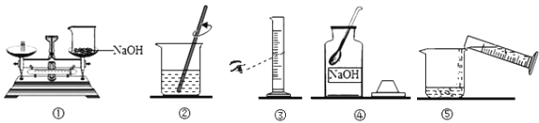
实验是学习化学中的重要手段,以下实验方法和操作中不能达到实验目的的是
选项 | 实验目的 | 实验方法和操作 |
A | 鉴别O2和CO2 | 分别伸入燃着的木条 |
B | 鉴别NaOH、NaCl | 取样于表面皿中,观察固体是否潮解 |
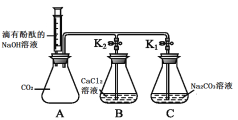
C | 除去NaCl溶液中混有的CaCl2 | 加适量K2CO3溶液、过滤 |
D | 除去FeSO4溶液中的CuSO4 | 加足量Fe粉,过滤 |
A. A B. B C. C D. D
 每课必练系列答案
每课必练系列答案化学研究物质及其变化,以下对物质和变化的解释正确的是
选项 | 事实 | 解释 |
A | 稀硫酸能导电 | 溶液中有自由移动的离子 |
B | 过氧化氢溶液分解出氧气 | 过氧化氢中含有氧分子 |
C | 金刚石、石墨性质存在明显差异 | 碳原子的结构不同 |
D | 氧气加压后变成液氧 | 氧分子的体积变小 |
A. A B. B C. C D. D
生活中常遇见铜制品生锈的情况.活动课上,同学们设计实验对铜锈进行了如下探究活动.
探究活动一:验证铜锈的组成
(查阅资料)
①铜锈为绿色,其主要成分是Cu2(OH)2CO3.
②白色的硫酸铜粉末遇水能变为蓝色.
③碳不与稀硫酸反应.
④氧化铜为黑色固体,能与稀硫酸反应生成硫酸铜溶液.
(进行实验1)
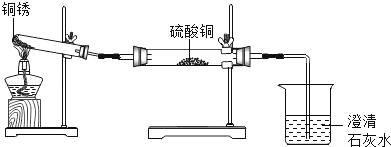
同学们设计了如图所示装置并进行实验.
实验操作 | 实验现象 | 实验结论 |
①按上图组装仪器,装入药品. ②加热铜锈,直至不再有气体产生,停止加热. | 绿色固体变为黑色;硫酸铜粉末变为蓝色;烧杯中液体变浑浊. | 加热铜锈生成的物质有__;铜锈由___元素组成;烧杯中发生反应的化学方程式为___. |
③冷却后,向试管中固体加入适量稀硫酸,稍加热. | 黑色固体溶解,溶液变为蓝色. |
探究活动二:探究铜生锈的条件
(进行实验2)
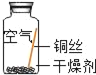
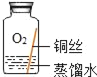
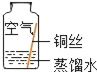
同学们进行了下面的4个实验,每天观察一次现象,一段时间后,发现只有实验4中的铜丝生锈了,且与水接触的部分生锈更明显.
序号 | 实验内容 | 实验结论 | 实验反思 |
实验1 |
| 在干燥环境中,铜不易生锈. | (1)实验2和3中使用的是经煮沸后迅速冷却的蒸馏水,其原因是___. (2)如果要证明铜生锈的快慢是否与二氧化碳的浓度有关,还需要补充的一个实验内容是___. |
实验2 |
| ___. | |
实验3 |
| ___. | |
实验4 |
| 铜生锈的条件是___. |




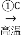 Si(粗)
Si(粗)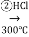 SiHCl3
SiHCl3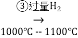 Si(纯)
Si(纯)