11.化学学科需要借助化学专用语言来描述,下列化学用语与其含义相符的是( )
| A. | 两个氧原子:O2 | B. | 一氧化碳分子:Co | ||
| C. | 三氧化硫:SO3 | D. | 碳酸根离子:CO3-2 |
10.某兴趣小组在制取氧气的实验过程中,小芳在实验时,误把氧化铜当作二氧化锰放入加热,结果发现也能较快产生氧气,于是进行如下探究:
【猜想Ⅰ】除二氧化锰、氧化铜外,氧化铁(Fe2O3)也可以作氯酸钾分解的催化剂.
【设计实验】
按下表进行实验,并测定开始产生气体时的温度(开始产生气体的温度越低,表示反应速度越快).
【数据和结论】
(1)选取实验①①(填写试验编号)进行对比,可以证明猜想Ⅰ合理;
(2)实验所用的三种物质中,催化效果最好的是②二氧化锰.
【反思】
(3)若要证明氧化铁是该反应的催化剂,还需要在实验丁中的剩余物加入氯酸钾,再次加热,并测定开始产生气体时的温度.以上操作是验证氧化铁在化学反应前后的③质量是否改变.除此之外,还需要验证④化学性质是否改变(不要填写具体的操作)小林在实验时,联想到了渔民用过氧化钙(CaO2)增加鱼池中的含氧量,提出猜想Ⅱ.
【猜想Ⅱ】过氧化钙与水反应可制取氧气.
实验结论:过氧化钙与水反应⑤不能(填“能”或“不能”)用于实验室制取氧气.
【分析与反思】
(1)过氧化钙与水反应虽然没有快速收集到大量氧气,但由此实验现象,小林认为渔民用过氧化钙做增氧剂的主要原因是⑥过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂.
(2)同学们对过氧化钙与水反应的生成物猜想如下:A:氢氧化钙和氧气 B:碳酸钙和氧气
你认为猜想⑦②(填序号)一定是错误的,理由是⑧化学反应前后元素的种类不变,而反应前没有碳元素.
(3)【计算】该兴趣小组的同学们取了100克过氧化钙来制取氧气,试计算出100克过氧化钙中氧元素的质量.
【猜想Ⅰ】除二氧化锰、氧化铜外,氧化铁(Fe2O3)也可以作氯酸钾分解的催化剂.
【设计实验】
按下表进行实验,并测定开始产生气体时的温度(开始产生气体的温度越低,表示反应速度越快).
| 实验编号 | 实验药品 | 分解温度(℃) |
| 甲 | 氯酸钾 | 580 |
| 乙 | 氯酸钾和二氧化锰(质量比1:1) | 350 |
| 丙 | 氯酸钾和氧化铜(质量比1:1) | 370 |
| 丁 | 氯酸钾和氧化铁(质量比1:1) | 390 |
(1)选取实验①①(填写试验编号)进行对比,可以证明猜想Ⅰ合理;
(2)实验所用的三种物质中,催化效果最好的是②二氧化锰.
【反思】
(3)若要证明氧化铁是该反应的催化剂,还需要在实验丁中的剩余物加入氯酸钾,再次加热,并测定开始产生气体时的温度.以上操作是验证氧化铁在化学反应前后的③质量是否改变.除此之外,还需要验证④化学性质是否改变(不要填写具体的操作)小林在实验时,联想到了渔民用过氧化钙(CaO2)增加鱼池中的含氧量,提出猜想Ⅱ.
【猜想Ⅱ】过氧化钙与水反应可制取氧气.
| 实验装置 | 实验主要过程 |
 | 第一步,检查装置气密性. 第二步,加入过氧化钙和水后,有少量细小气泡缓慢放出,在导管口几乎收集不到气体.该装置放置到第二天,集气瓶中只收集到极少量气体,震荡试管后仍有少量细小气泡缓慢放出. |
【分析与反思】
(1)过氧化钙与水反应虽然没有快速收集到大量氧气,但由此实验现象,小林认为渔民用过氧化钙做增氧剂的主要原因是⑥过氧化钙在水中持续、缓慢放出氧气,所以可以作为增氧剂.
(2)同学们对过氧化钙与水反应的生成物猜想如下:A:氢氧化钙和氧气 B:碳酸钙和氧气
你认为猜想⑦②(填序号)一定是错误的,理由是⑧化学反应前后元素的种类不变,而反应前没有碳元素.
(3)【计算】该兴趣小组的同学们取了100克过氧化钙来制取氧气,试计算出100克过氧化钙中氧元素的质量.
9.从分子的角度分析并解释下列事实,其中不正确的是( )
| A. | 闻到酒香--分子在不断运动 | |
| B. | 水蒸发成水蒸气--分子的大小发生变化 | |
| C. | 氢气在空气中燃烧--分子种类改变 | |
| D. | 100升气体被压缩到1升钢瓶中--分子间有间隔 |
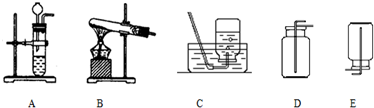
8.实验室常用下列装置来制取氧气:

(1)写出图中有标号仪器的名称:a酒精灯、b铁架台;
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),其中二氧化锰起催化作用.
(3)用高锰酸钾制取氧气时,发生反应的文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气
(4)用E装置收集氧气的依据是氧气密度比空气大,检验氧气是否集满的方法是把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下氨气是一种无色、有刺激性气味的气体,密度比空气小.氨气极易溶于水.由此可知制取并收集氨气,应该从上图中选择的发生装置是A,收集装置是D.若用F装置收集氨气,氨气应从n(填“m”或“n”)端进入.
(6)某研究小组对用H2O2分解生成H2O和O2的实验条件进行探究.他们进行了以下实验:
①往盛有5mL 5% H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5mL w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5mL w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②、③中反应后试管中仍分别含有a g MnO2和a g Fe2O3.
问题:
(1)MnO2、Fe2O3在上述反应中的作用是催化剂.
(2)实验 ②、③中H2O2的浓度(w%)以5%为宜.
研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究,下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需的时间
问题:(3)从上表中能得出哪些结论?二氧化锰的催化效果比氧化铁的催化效果好,浓度越大,分解速率越快.

(1)写出图中有标号仪器的名称:a酒精灯、b铁架台;
(2)用双氧水和二氧化锰来制取氧气时,可选用的发生装置是B(填序号),其中二氧化锰起催化作用.
(3)用高锰酸钾制取氧气时,发生反应的文字表达式为高锰酸钾$\stackrel{加热}{→}$锰酸钾+二氧化锰+氧气
(4)用E装置收集氧气的依据是氧气密度比空气大,检验氧气是否集满的方法是把带火星的木条放在集气瓶口,如果带火星的木条复燃,说明已经收集满.
(5)实验室常用氯化铵固体与碱石灰固体共热来制取氨气.常温下氨气是一种无色、有刺激性气味的气体,密度比空气小.氨气极易溶于水.由此可知制取并收集氨气,应该从上图中选择的发生装置是A,收集装置是D.若用F装置收集氨气,氨气应从n(填“m”或“n”)端进入.
(6)某研究小组对用H2O2分解生成H2O和O2的实验条件进行探究.他们进行了以下实验:
①往盛有5mL 5% H2O2溶液的试管中,伸入带火星的木条,木条不复燃.
②往盛有5mL w% H2O2溶液的试管中,加入a g MnO2,伸入带火星的木条,木条复燃.
③往盛有5mL w% H2O2溶液的试管中,加入a g Fe2O3,伸入带火星的木条,木条复燃.
④经检验,②、③中反应后试管中仍分别含有a g MnO2和a g Fe2O3.
问题:
(1)MnO2、Fe2O3在上述反应中的作用是催化剂.
(2)实验 ②、③中H2O2的浓度(w%)以5%为宜.
研究小组还对溶液浓度、催化剂的种类等实验条件进行了探究,下表选取了部分实验数据:用足量等体积H2O2溶液制取相同体积O2所需的时间
| 浓度 时间(min) 条件 | 30% H2O2 | 15% H2O2 | 5% H2O2 |
| 加入a g MnO2 | 0.2 | 0.8 | 2.0 |
| 加入a g Fe2O3 | 7.0 | 9.0 | 16.0 |
2.下列属于分解反应的是( )
0 168163 168171 168177 168181 168187 168189 168193 168199 168201 168207 168213 168217 168219 168223 168229 168231 168237 168241 168243 168247 168249 168253 168255 168257 168258 168259 168261 168262 168263 168265 168267 168271 168273 168277 168279 168283 168289 168291 168297 168301 168303 168307 168313 168319 168321 168327 168331 168333 168339 168343 168349 168357 211419
| A. | 红磷燃烧:P+O2$\stackrel{点燃}{→}$P2O5 | B. | 硫燃烧:S+O2$\stackrel{点燃}{→}$SO2 | ||
| C. | 木炭燃烧:C+O2$\stackrel{点燃}{→}$CO2 | D. | 双氧水制氧气:H2O2$\stackrel{MnO_{2}}{→}$H2O+O2 |
 、
、 、
、 分别表示三种元素的原子,那么有下面四幅图表示构成物质的粒子.
分别表示三种元素的原子,那么有下面四幅图表示构成物质的粒子.