20.四氧化三铁可用于医疗器械、电子等工业.某实验兴趣小组从工厂采集废液(含FeSO4和少量ZnSO4、MgSO4),进行四氧化三铁的制备实验.
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表.
(2)25℃时,Zn(OH)2可溶于pH>10.5的碱溶液.
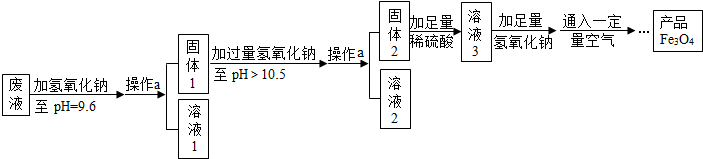
(3)制备Fe3O4的实验流程如图:
【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为(写一个即可)2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4【或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4】.
(2)溶液1所含溶质有(至少写两种)硫酸镁、硫酸钠;溶液3所含溶质的主要成分为硫酸亚铁.
(3)该实验取废液100g,最终得到产品四氧化三铁质量为2.32g,则原废液中硫酸亚铁溶质的质量分数不低于4.56%(精确到0.01%).
【阅读资料】
(1)25℃时,氢氧化物沉淀的pH范围如表.
| Zn(OH)2 | Fe(OH)2 | Mg(OH)2 | |
| 开始沉淀的pH | 5.7 | 7.6 | 10.4 |
| 沉淀完全的pH | 8.0 | 9.6 | 12.4 |
(3)制备Fe3O4的实验流程如图:

【回答问题】
(1)往废液中加入氢氧化钠溶液生成沉淀的化学方程式为(写一个即可)2NaOH+ZnSO4═Zn(OH)2↓+Na2SO4【或2NaOH+FeSO4═Fe(OH)2↓+Na2SO4】.
(2)溶液1所含溶质有(至少写两种)硫酸镁、硫酸钠;溶液3所含溶质的主要成分为硫酸亚铁.
(3)该实验取废液100g,最终得到产品四氧化三铁质量为2.32g,则原废液中硫酸亚铁溶质的质量分数不低于4.56%(精确到0.01%).
19.下列的陈述中Ⅰ、Ⅱ的因果关系正确的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 生石灰易与水反应 | 生石灰常用作食品干燥剂 |
| B | 氢气是最轻的气体 | 点燃氢气前要验纯 |
| C | 二氧化碳用于灭火 | 二氧化碳没有毒性 |
| D | 取液时试剂瓶塞倒放在桌面上 | 液体药品盛放在细口瓶 |
| A. | A | B. | B | C. | C | D. | D |
18.下列实验操作正确的是( )
| A. |  | B. |  | C. |  | D. |  |
17.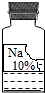 实验室有一瓶保存不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,可能是NaCl、NaOH、Na2CO3、NaHCO3溶液中的一种.同学们很感兴趣,决定对其成分进行探究:
实验室有一瓶保存不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,可能是NaCl、NaOH、Na2CO3、NaHCO3溶液中的一种.同学们很感兴趣,决定对其成分进行探究:
(1)【查阅资料】室温(20℃)时,四种物质的溶解度的数据如表:
【得出结论】某同学根据试剂瓶标注的溶质质量分数10%和上表中的溶解度的数据判断,这瓶试剂不可能是上述溶液中的NaHCO3溶液.
(2)【设计实验】为了进一步确定该溶液是何种溶液,该同学进行了以下实验操作,请你帮助其补充完整下列实验方案,叙述实验操作、预期现象与结论.
 实验室有一瓶保存不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,可能是NaCl、NaOH、Na2CO3、NaHCO3溶液中的一种.同学们很感兴趣,决定对其成分进行探究:
实验室有一瓶保存不当的试剂(如图),其残缺的标签中只剩下“Na”和“10%”字样.已知它是无色液体,可能是NaCl、NaOH、Na2CO3、NaHCO3溶液中的一种.同学们很感兴趣,决定对其成分进行探究:(1)【查阅资料】室温(20℃)时,四种物质的溶解度的数据如表:
| 物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
| 溶解度g | 36 | 109 | 215 | 9.6 |
(2)【设计实验】为了进一步确定该溶液是何种溶液,该同学进行了以下实验操作,请你帮助其补充完整下列实验方案,叙述实验操作、预期现象与结论.
| 实验操作 | 预期现象与结论 |
| 取少量样品溶液于试管中,滴加几滴酚酞试液. | 若无明显现象,则原溶液为NaCl 若溶液由无色变成红色,则原溶液为NaOH或Na2CO3 |
| 再取少量样品溶液于试管中,滴加少量稀盐酸. | 若试管中产生气泡,则原溶液为Na2CO3 若无明显现象,则原溶液为NaOH |
15.某学校开展科学实验探究活动.
(1)同学们在探究酸碱盐物质的性质时,进行了如下实验:
(2)某同学取一块表面完全锈蚀的生铁片进行了以下探究:
.
0 166057 166065 166071 166075 166081 166083 166087 166093 166095 166101 166107 166111 166113 166117 166123 166125 166131 166135 166137 166141 166143 166147 166149 166151 166152 166153 166155 166156 166157 166159 166161 166165 166167 166171 166173 166177 166183 166185 166191 166195 166197 166201 166207 166213 166215 166221 166225 166227 166233 166237 166243 166251 211419
(1)同学们在探究酸碱盐物质的性质时,进行了如下实验:
| 步骤 | 操作 | 现象 | 分析与结论 |
| ① | 分别向盛有NaOH溶液、KOH溶液的A,B两试管中加入CuSO4溶液. | 两支试管均有蓝色沉淀生成 | 不同的碱溶液都含有OH-(填化学符号)所以不同的碱都有相似的化学性质. |
| ② | 用玻璃棒分别蘸取稀硫酸和浓硫酸于白纸A,B上,片刻. | 白纸A没明显现象;白纸B变黑(生成黑色的炭) | 同种酸,由于浓度不同,它们性质不完全相同 |
| 步骤 | 操作 | 现象 | 结论 |
| ① | 取适量固体于试管中加热,用一干冷玻片置于试管口上方. | 玻璃片上有小水珠 | 固体中含有H2O |
| ② | 取适量固体于试管中,加入足量的稀盐酸,观察溶液颜色. | 溶液呈黄色 | 固体中含有Fe2O3 |
| ③ | 收集步骤②试管中产生的气体,点燃. | 有爆鸣声 | 固体中含有Fe(填化学式) |
| ④ | 将上面反应后的混合液过滤. | 有黑色固体 | 黑色固体的主要成份 是C(填化学式) |

