15.已知30%的过氧化氢水溶液中氢元素的质量分数为9.54%.向这种溶液中加入少量的二氧化锰,充分反应后,过滤,所得液体中氢元素的质量分数约为( )
| A. | 11.11% | B. | 9.54% | C. | 5.88% | D. | 16.70% |
14.某校化学课堂围绕课本《实验活动6:酸、碱的化学性质》开展自主探究活动,以下是探究片段,请你参与学习.
(1)向装有生锈铁钉的试管中加入稀盐酸,观察到铁锈逐渐消失,因此盐酸常用于金属表面除锈,该反应的化学方程式为:6HCl+Fe2O3=2FeCl3+3H2O;
(2)在进行盐酸中和氢氧化钠溶液实验时,某一小组忘记向氢氧化钠溶液中滴加酚酞试液,因此未观察到明显现象.该小组同学对此时反应后所得溶液的成分产生疑问;
[假设猜想]针对疑问,第一组同学的猜想如下:
猜想一:只有NaCl 猜想二:有NaCl和HCl
猜想三:有NaCl和NaOH 猜想四:有NaCl、HCl和NaOH
第二组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是猜想四;
[实验探究]①第三组同学取少量该溶液于试管中,滴加酚酞溶液,无明显变化,则溶液中一定没有氢氧化钠;
②为验证其余猜想,第四组同学分别取该溶液样品按下列方案探究:
[得出结论]通过比较分析,同学们一致确定猜想二是正确的;
[评价反思]①老师对同学们能用多种方法进行探究给予肯定,同时指出方案二是错误的,原因是氯化钠中的氯离子也会与硝酸银生成白色沉淀;②小明发现,排除不合理猜想后,只做一次实验就能同时验证其余猜想,此实验方法是:滴入石蕊试液,观察溶液颜色;
[交流讨论]中和反应在日常生活和工农业生产中有广泛应用,请你举一个实例说明:改良酸性土壤.
(1)向装有生锈铁钉的试管中加入稀盐酸,观察到铁锈逐渐消失,因此盐酸常用于金属表面除锈,该反应的化学方程式为:6HCl+Fe2O3=2FeCl3+3H2O;
(2)在进行盐酸中和氢氧化钠溶液实验时,某一小组忘记向氢氧化钠溶液中滴加酚酞试液,因此未观察到明显现象.该小组同学对此时反应后所得溶液的成分产生疑问;
[假设猜想]针对疑问,第一组同学的猜想如下:
猜想一:只有NaCl 猜想二:有NaCl和HCl
猜想三:有NaCl和NaOH 猜想四:有NaCl、HCl和NaOH
第二组同学对以上猜想提出质疑,认为有一种猜想是不合理的.你认为不合理的猜想是猜想四;
[实验探究]①第三组同学取少量该溶液于试管中,滴加酚酞溶液,无明显变化,则溶液中一定没有氢氧化钠;
②为验证其余猜想,第四组同学分别取该溶液样品按下列方案探究:
| 方案 | 实验操作 | 实验现象 | 实验结论 |
| 方案一 | 往溶液中加碳酸钠 | 有气泡产生 | 溶液中有HCl |
| 方案二 | 往溶液中滴加AgNO3溶液 | 产生白色沉淀 | 溶液中有HCl |
[评价反思]①老师对同学们能用多种方法进行探究给予肯定,同时指出方案二是错误的,原因是氯化钠中的氯离子也会与硝酸银生成白色沉淀;②小明发现,排除不合理猜想后,只做一次实验就能同时验证其余猜想,此实验方法是:滴入石蕊试液,观察溶液颜色;
[交流讨论]中和反应在日常生活和工农业生产中有广泛应用,请你举一个实例说明:改良酸性土壤.
10.用量筒取10ml水时,某同学读数时是俯视读数,则所量取水的实际体积( )
| A. | =10ml | B. | <10ml | C. | >10ml | D. | 无法估计 |
9.下列化学反应中,既是化合反应又是氧化反应的是( )
0 165916 165924 165930 165934 165940 165942 165946 165952 165954 165960 165966 165970 165972 165976 165982 165984 165990 165994 165996 166000 166002 166006 166008 166010 166011 166012 166014 166015 166016 166018 166020 166024 166026 166030 166032 166036 166042 166044 166050 166054 166056 166060 166066 166072 166074 166080 166084 166086 166092 166096 166102 166110 211419
| A. | 镁+氧气$\stackrel{点燃}{→}$ 氧化镁 | B. | 氧化汞 $\stackrel{加热}{→}$ 汞+氧气 | ||
| C. | 石蜡+氧气$\stackrel{点燃}{→}$ 二氧化碳+水 | D. | 水 $\stackrel{通电}{→}$ 氢气+氧气 |
 铁、铜、镁、锌是几种金属活动性不同的金属,将他们同时放入稀盐酸中,出现了如图表示的情形.请分析它们的表白后填空.
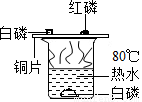
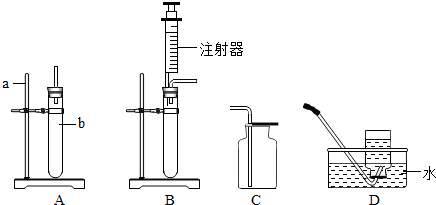
铁、铜、镁、锌是几种金属活动性不同的金属,将他们同时放入稀盐酸中,出现了如图表示的情形.请分析它们的表白后填空. 实验探究--测定空气中氧气的含量.装置如图所示:
实验探究--测定空气中氧气的含量.装置如图所示: