13.某两种物质在一定条件下发生化学反应的微观示意图如图所示(其 分别表示两种不同的原子)对上述反应,下列说法正确的是( )
分别表示两种不同的原子)对上述反应,下列说法正确的是( )

 分别表示两种不同的原子)对上述反应,下列说法正确的是( )
分别表示两种不同的原子)对上述反应,下列说法正确的是( )
| A. | 反应物都是化合物 | B. | 反应属于分解反应 | ||
| C. | 生成物可能是氧化物 | D. | 反应前后分子种类不同 |
12.金属是一种重要的材料,人类的生活和生产都离不开金属,全世界每年因生锈损失的钢铁,约占世界年产量的十分之一.
(1)根据图一的应用实例,试说出金属具有的一点物理性质导电性(或导热性等);
(2)铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,原因是铝的表面形成致密的氧化膜;
(3)表中不同的金属被开发、利用的年代不同,决定这一先后顺序的关键因素是A;

A.金属的活动性 B.金属的导电性
C.金属的延展性 D.地壳中金属元素的含量
(4)用质量相等的镁粉和铝粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应,产生氢气的质量和反应所用时间的关系如图二所示.则下列说法中正确的是AB;
A.曲线a、b分别表示镁、铝的反应情况 B.盐酸均反应完,镁恰好完全反应,铝剩余
C.盐酸均反应完,镁、铝也恰好完全反应 D.镁、铝都反应完,盐酸有剩余
(5)联想到工业上用铁矿石冶炼铁,他们在实验室用CO还原氧化铁,实验如图三所示:

①A、B处发生的现象分别是A固体由红变黑;B石灰水变浑浊.
②为了防止溶液倒吸,本实验停止加热前是否要先断开A和B的连接处?不需要(填“需要”或“不需要”),理由是气体会一直通到装置冷却,不会发生倒吸.
(6)兴趣小组的同学又准确称取了11.5克生铁样品,放入装有100.0g稀硫酸(足量)的烧杯中(烧杯质量为55.0g).在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如表.
求:
①反应中产生氢气0.4克;
②原生铁样品中铁的质量分数.(写出计算的过程,结果精确到0.1%)
(1)根据图一的应用实例,试说出金属具有的一点物理性质导电性(或导热性等);
(2)铝的活动性比铁强,但铝在空气中却表现出良好的抗腐蚀性,原因是铝的表面形成致密的氧化膜;
(3)表中不同的金属被开发、利用的年代不同,决定这一先后顺序的关键因素是A;

A.金属的活动性 B.金属的导电性
C.金属的延展性 D.地壳中金属元素的含量
(4)用质量相等的镁粉和铝粉,分别与溶质质量分数相同、等质量的稀盐酸充分反应,产生氢气的质量和反应所用时间的关系如图二所示.则下列说法中正确的是AB;
A.曲线a、b分别表示镁、铝的反应情况 B.盐酸均反应完,镁恰好完全反应,铝剩余
C.盐酸均反应完,镁、铝也恰好完全反应 D.镁、铝都反应完,盐酸有剩余
(5)联想到工业上用铁矿石冶炼铁,他们在实验室用CO还原氧化铁,实验如图三所示:

①A、B处发生的现象分别是A固体由红变黑;B石灰水变浑浊.
②为了防止溶液倒吸,本实验停止加热前是否要先断开A和B的连接处?不需要(填“需要”或“不需要”),理由是气体会一直通到装置冷却,不会发生倒吸.
(6)兴趣小组的同学又准确称取了11.5克生铁样品,放入装有100.0g稀硫酸(足量)的烧杯中(烧杯质量为55.0g).在化学反应过程中对烧杯(包括溶液和残余固体)进行了四次称量,记录如表.
| 反应时间 | t0 | t1 | t2 | t3 |
| 烧杯和药品的质量/g | 166.5 | 166.3 | 166.1 | 166.1 |
①反应中产生氢气0.4克;
②原生铁样品中铁的质量分数.(写出计算的过程,结果精确到0.1%)
11. 小明设计了趣味实验装置(如图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )(滴入的液体的体积忽略不计)
小明设计了趣味实验装置(如图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )(滴入的液体的体积忽略不计)
 小明设计了趣味实验装置(如图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )(滴入的液体的体积忽略不计)
小明设计了趣味实验装置(如图),其气密性良好.若要使B中尖嘴导管有“喷泉”产生,则A中加入的固体和液体可能是( )(滴入的液体的体积忽略不计)| A. | 氯化钠和水 | B. | 硝酸铵和水 | ||
| C. | 二氧化锰和过氧化氢溶液 | D. | 氢氧化钠和水 |
10.下列现象不能用质量守恒定律解释的是( )
| A. | 铁钉生锈后质量增加 | B. | 煤燃烧后质量减轻 | ||
| C. | 双氧水分解后质量减少 | D. | 10g的冰融化后变为10g的水 |
8.相对原子质量的大小主要决定于原子的( )
0 163273 163281 163287 163291 163297 163299 163303 163309 163311 163317 163323 163327 163329 163333 163339 163341 163347 163351 163353 163357 163359 163363 163365 163367 163368 163369 163371 163372 163373 163375 163377 163381 163383 163387 163389 163393 163399 163401 163407 163411 163413 163417 163423 163429 163431 163437 163441 163443 163449 163453 163459 163467 211419
| A. | 质子数 | B. | 电子数 | C. | 中子数 | D. | 质子数和中子数 |
 新型的风能、太阳能路灯能“吸住太阳光”、“揽住风力”.请回答下列问题:
新型的风能、太阳能路灯能“吸住太阳光”、“揽住风力”.请回答下列问题:
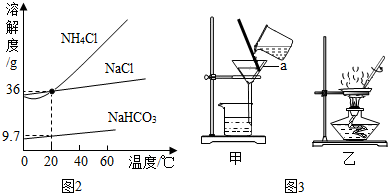
 如图是a、b、c三种物质的溶解度曲线,请你回答:
如图是a、b、c三种物质的溶解度曲线,请你回答: