已知某合金粉末除铝外,还含有铁、铜中的一种或两种.某兴趣小组在老师的指导下,对合金粉末中铁、铜的存在情况进行了探究.
【查阅资料】铝与氢氧化钠溶液反应方程式为2Al+2NaOH+2H2O=2NaAlO2+3H2↑(产物NaAlO2溶于水);Fe、Cu不与氢氧化钠溶液反应.
【猜想】猜想1:该合金粉末中除铝外,还含有铁.
猜想2:该合金粉末中除铝外,还含有________(填名称).
猜想3:该合金粉末中除铝外,还含有铁、铜.
【实验探究】下列实验仅供选择的试剂:10%盐酸、30%NaOH溶液.
| 实验方案 | 实现现象 | 结论 |
| ①取一定量的合金粉末,加过量的________,充分反应后过滤,滤渣备用. | 粉末部分溶解,并有气体放出. | 合金中一定含有________. |
| ②取步骤①所得滤渣,加过量的________,充分反应. | 滤渣部分溶解,并有气体放出,溶液呈浅绿色. | 合金中一定含有________. |
【反思】一般来说,活泼金属能与盐酸等酸反应,而铝与酸、碱都能反应,说明铝具有特殊的性质.写出铝与稀盐酸反应的化学方程式________.
向10mL未知浓度的NaOH溶液中加入10mL未知浓度的CuSO4溶液,有蓝色絮状沉淀生成,有关的化学方程式为:______.请设计简单的实验初步判断:溶液中的NaOH和CuSO4是否已经完全反应,将实验探究的步骤和可能观察到的现象及结论填写在下列实验报告中.
| 实验步骤 | 观察到的现象 | 结 论 |
| (1)过滤、取滤液观察 (2)取滤液样品于试管中,加入几滴无色酚酞试液 | (1)①滤液呈蓝色 ②滤液无色 (2)①若酚酞变红 ②______ | (1)①______ ②______ (2)①______ ②______ |
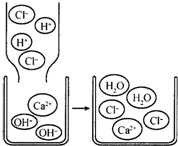
 在稀硫酸中加入下列哪种物质,溶液的导电性会出现如图所示的变化?
在稀硫酸中加入下列哪种物质,溶液的导电性会出现如图所示的变化?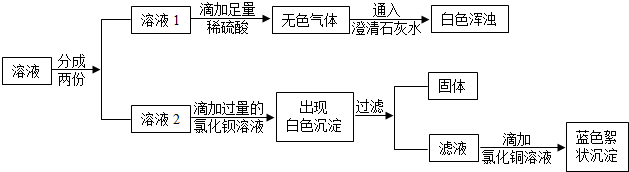
 “世界是物质的,而物质是由粒子构成的”“化学变化的实质是粒子重新组合的过程”等都是化学学科中的重要观点.依据给定元素的化合价,从
“世界是物质的,而物质是由粒子构成的”“化学变化的实质是粒子重新组合的过程”等都是化学学科中的重要观点.依据给定元素的化合价,从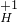 、
、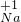 、
、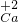 、
、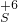 、
、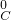 、
、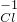 、
、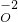 七种元素中任选一种或几种元素组成物质,回答下列问题.
七种元素中任选一种或几种元素组成物质,回答下列问题. 化学兴趣小组同学对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请按要求填空:
化学兴趣小组同学对“金属活动性顺序”从内容、规律以及应用等方面进行了总结,请按要求填空: 氧气的验满
氧气的验满


