不少溶洞里的地下河水是含有MgCl2和CaCl2的硬水.下表是某化学兴趣小组设计的软化硬水实验方案,请你一起来完成.
| 实验操作 | 现象 | 结论或化学方程式 |
| 步骤Ⅰ:取少量硬水样品于试管中,向其中滴加Ca(OH)2溶液,直到反应完全. | 有白色沉淀产生. | MgCl2+Ca(OH)2=Mg(OH)2↓+CaCl2 |
| 步骤Ⅱ:向上述试管中滴加 ________溶液,直到反应完全. | ________ | 化学方程式:________ |
| 步骤Ⅲ:________ (填操作 名称). | 除去沉淀物. | 得到澄清滤液. |
| 步骤Ⅳ:用两试管取等量的上述滤液和原硬水样品,分别滴加 ________,振荡. | 盛有滤液的试管中________. | 证明硬水已软化. |
有一种石灰石样品的成分是CaCO3和SiO2(已知SiO2既不溶于水也不与盐酸反应).现将一定量的石灰石样品放入烧杯中,再将100g稀盐酸分4次加入烧杯中,每次均充分反应.实验数据记录如下:
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸的质量/g | 25 | 25 | 25 | 25 |
| 充分反应后剩余固体质量/g | 7 | 4 | 2 | M |
(2)该石灰石样品中碳酸钙的质量分数.
(3)生成二氧化碳的总质量.
 胃酸过多须服用抗酸药物(能与盐酸反应).右图为某抗酸药说明书部分内容.兴趣小组对该药物开展如下探究.回答下列问题:
胃酸过多须服用抗酸药物(能与盐酸反应).右图为某抗酸药说明书部分内容.兴趣小组对该药物开展如下探究.回答下列问题: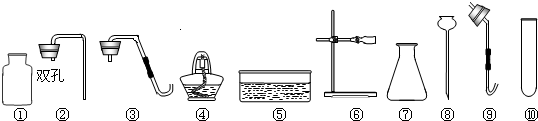
 (1)利用上述仪器及药品制取某一气体,所需仪器有______ (填序号);制取该气体的化学方程式______
(1)利用上述仪器及药品制取某一气体,所需仪器有______ (填序号);制取该气体的化学方程式______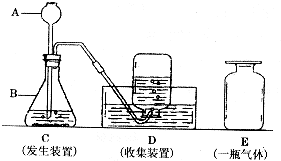 实验是化学学科的核心内容之一,实验装置的选择、实验操作重在对原理的理解.图示是实验室制取氢气、氧气和二氧化碳三种气体中的某一气体的装置简图.
实验是化学学科的核心内容之一,实验装置的选择、实验操作重在对原理的理解.图示是实验室制取氢气、氧气和二氧化碳三种气体中的某一气体的装置简图.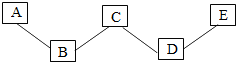 已知A、B、C、D、E分别是稀盐酸、氢氧化钠溶液、硫酸铜溶液、氧化铁和一氧化碳中的一种,E是实验室一种常见溶液,它们之间的关系如图所示,“─”两端的物质在一定条件下可以反应.请回答:
已知A、B、C、D、E分别是稀盐酸、氢氧化钠溶液、硫酸铜溶液、氧化铁和一氧化碳中的一种,E是实验室一种常见溶液,它们之间的关系如图所示,“─”两端的物质在一定条件下可以反应.请回答: