将4.87g部分氧化的锌片溶于50g稀H2SO4中,恰好完全反应,反应称得溶液质量为54.77g.
求:
(1)锌片中单质锌的质量.
(2)原稀H2SO4中溶质的质量分数.
(3)生成物溶液中溶质的质量分数.
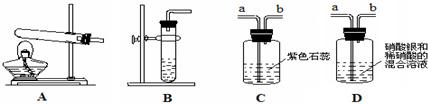
取四朵用石蕊试剂染成紫色的干燥纸花进行如下操作,能够观察到纸花变红的有________;可能变成其它颜色的是________.
①喷石灰水 ②喷水 ③直接放入CO2中 ④喷水后放入CO2中 ⑤喷稀硫酸.
某兴趣小组同学为证明NaOH溶液与稀盐酸发生了中和反应,从不同角度设计了如下实验方案,并进行实验.
I、实验方案
方案一:先用pH试纸测定NaOH溶液的pH,再滴加盐酸,并不断振荡溶液,同时测定混合溶液的pH,测得的pH逐渐变小直到pH小于7,则证明NaOH溶液与稀盐酸发生了化学反应.
(1)反应后,所得溶液显______性(填“酸”、“碱”或“中”)
(2)用pH试纸测定NaOH溶液pH时,正确的操作是:______.
(3)简述强调“测得的pH小于7”的理由:______.
方案二:化学反应中通常伴随有能量的变化,可借助反应前后的温度变化来判断反应的发生.如果NaOH溶液与稀盐酸混合前后温度有变化,则证明发生了化学反应.
该组同学将不同浓度的盐酸和NaOH溶液各10克混合,用温度计测定室温下混合前后温度的变化,并记录了每次混合前后温度的升高值△t(如下表).
| 编号 | 盐酸 | NaOH溶液 | △t/℃ |
| 1 | 3.65% | 2.00% | 3.5 |
| 2 | 3.65% | 4.00% | x |
| 3 | 7.30% | 8.00% | 14 |
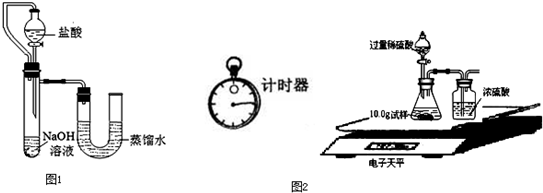
(5)某同学在没使用温度计的情况下,通过图1所示装置完成了实验.则该同学根据实验现象:______,判断NaOH溶液与稀盐酸发生了中和反应.
II、实验中的意外情况
在实验过程中,他们发现盛放NaOH溶液的试剂瓶瓶口和橡皮塞上出现了白色粉末.他们依据所学的化学知识,对这种白色粉末的成分作了如下猜想:①可能是NaOH;②可能是Na2CO3; ③可能是NaOH和Na2CO3.
(6)小明同学取白色粉末少许,溶于水后,先向溶液中加入足量的______溶液,看到白色沉淀产生,然后向上层清液中加入酚酞试液,看到溶液呈红色,验证了猜想③是正确的.
(7)为了进一步研究,三位同学取了10.0g上述样品,利用电子天平共同做了图所示的实验.
实验数据记录如下:
| 称 量 项 目 | 称 量 时 间 | 质量(g) |
| 试样 | 10.00 | |
| 装置+稀硫酸质量 | 241.20 | |
| 装置+稀硫酸质量+试样 | 反应开始后15秒 | 249.20 |
| 装置+稀硫酸质量+试样 | 反应开始后35秒 | 249.00 |
| 装置+稀硫酸质量+试样 | 反应开始后55秒 | 249.00 |
(8)有同学提出按上述实验所测得试样中Na2CO3质量分数会偏小,该同学的理由是(实验操作均正确):______.
 ”和“
”和“ ”分别表示不同原子.
”分别表示不同原子.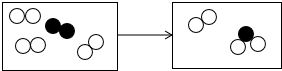
 B.
B. C.
C.