下列物质之间,不能发生反应的是
| A.锌与硫酸铜溶液 | B.铝与硝酸银溶液 |
| C.铜与硫酸锌溶液 | D.铁与硝酸银溶液 |
有等质量的两种金属A和B,前者放入质量分数为10%的稀硫酸中,后者放入质量分数为20%的稀盐酸中,产生氢气的质量随时间变化曲线如图所示。下列说法错误的是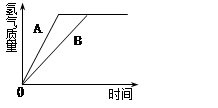
| A.产生氢气物质的量相等 | B.金属的活泼性A>B |
| C.酸过量,金属质量不足 | D.A与硫酸反应更为剧烈 |
把过量的铁粉加入到H2SO4和CuSO4的混合溶液中,充分反应后过滤,有关此实验的说法,不正确的是
| A.滤液中只含有FeSO4 |
| B.滤液中含有FeSO4和H2SO4 |
| C.过滤所得固体是Fe和Cu |
| D.所发生的反应都是置换反应 |
根据你的实验经验,下列几种金属投入到稀硫酸中产生氢气速度最快的是
| A.铜 | B.锌 | C.镁 | D.铁 |
若金属锰(Mn)在金属活动性顺序中位于铝和锌之间,则下列反应不正确的是( )
| A.Mn+2HCl =MnC12+H2↑ |
| B.Mg +MnSO4= MgSO4+Mn |
| C.Mn+Cu(NO3)2=Mn(NO3)2+Cu |
| D.Fe+MnSO4 =FeSO4+Mn |
下列关于“铁、铜、锌金属性强弱”的探究实验设计中,不合理的是 ( )
| A.先分别把金属铁、铜、锌加入稀盐酸中;再将金属铁加入硫酸锌溶液中 |
| B.分别将金属锌和铜加入到硫酸铁溶液中 |
| C.将金属铁分别加入硫酸锌溶液和硫酸铜溶液中 |
| D.分别将金属锌和铜加入到氯化亚铁溶液中 |
向含有AgNO3、Cu(NO3)2的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的固体中滴加稀硫酸,有气体生成,则滤出的固体一定为
| A.Ag、Cu两种单质的混合物 | B.Cu、Fe两种单质的混合物 |
| C.Ag、Fe两种单质的混合物 | D.Ag、Cu、 Fe三种单质的混合物 |
把某稀硫酸分为等体积的两份,放入两个烧杯中,分别加入等质量的甲、乙两种金属,反应后金属都没有剩余。产生H2的质量随时间变化的趋势如图。下列说法正确的是( )
| A.甲的活动性比乙强 |
| B.甲的相对原子质量一定比乙小 |
| C.反应消耗等质量的硫酸 |
| D.反应消耗等质量的金属 |
某合金6 g与足量的稀硫酸充分反应后,如果生成0.2 g氢气,该合金中的元素可能是( )
| A.Zn和Fe | B.Cu和Au |
| C.Zn和Cu | D.Mg和Al |
下列说法符合图中漫画情景的是( )
| A.此反应可能是复分解反应 |
| B.若金属1是锌,金属2可能是银 |
| C.此反应可能是Cu+2AgCl=2Ag+CuCl2 |
| D.比较铁和铜的活动性强弱可以用硫酸镁溶液 |