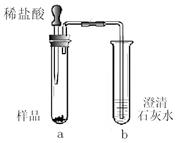
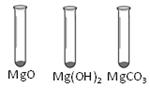
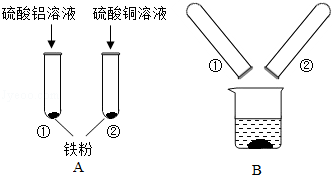
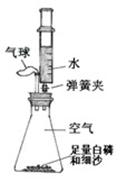
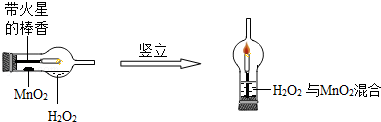
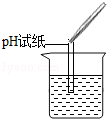
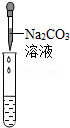
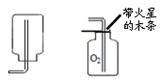
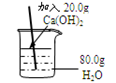
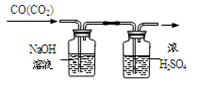
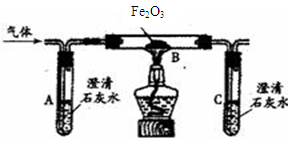
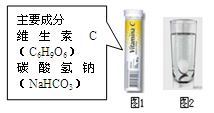
0 111299 111307 111313 111317 111323 111325 111329 111335 111337 111343 111349 111353 111355 111359 111365 111367 111373 111377 111379 111383 111385 111389 111391 111393 111394 111395 111397 111398 111399 111401 111403 111407 111409 111413 111415 111419 111425 111427 111433 111437 111439 111443 111449 111455 111457 111463 111467 111469 111475 111479 111485 111493 211419