1mol某化合物在2mol氧气中恰好完全燃烧,生成了44g二氧化碳和36克水,对该化合物的元素组成判断正确的是( )
| A、只含有碳、氢元素 | B、一定含有碳、氢元素,可能含有氧元素 | C、一定含有碳、氢、氧元素 | D、一定含碳、氧元素,可能含有氢元素 |
硝化甘油(C3H5N3O9)可用于治疗心绞痛.因为它在人体中被氧化成X气体;4C3H5N3O9+5O2═12X+12CO2+10H2O.下列有关说法不正确的是( )
| A、C3H5N3O9属于有机物 | B、C3H5N3O9各元素中氢元素质量分数最小 | C、X的化学式为NO | D、参加反应的C3H5N3O9和O2的质量比为4:5 |
下列符合质量守恒定律是( )
| A、木炭燃烧后变成灰烬,质量减少 | B、一定条件下,SO2和O2生成SO3,反应前后分子总数不变 | C、100g水加入100g酒精,成为总质量为200g的溶液 | D、8g H2完全燃烧生成8g H2O |
下列4个图象能正确反映对应变化关系是( )
| A | B | C | D |
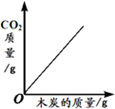 |  | 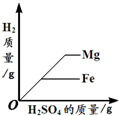 | 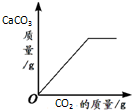 |
| 引燃密闭集气瓶中的木炭(过量) | 向盛有一定量碳酸钙粉末的烧杯中加入稀盐酸 | 向等质量的镁、铁两种金属中分别加入同浓度的足量稀硫酸 | 向盛有一定量的Ca(OH)2溶液的烧杯中通入CO2 |
| A、A | B、B | C、C | D、D |
人们常用金属器皿来盛水,也常用铁、铝或铜制的水壶来烧水,说明这几种金属与热水是不反应的,但金属钠却能与水发生以下反应:2Na+2H2O=2R+H2↑,而R是( )
| A、Na | B、Na2O | C、Na2O2 | D、NaOH |
科学研究表明,氨气在常压下就可液化为液氨,液氨可用作汽车的清洁燃料,其燃烧时的主要反应为
4NH3+3O2
2X+6H2O.下列说法中,不正确的是( )
4NH3+3O2
| ||
| A、氨气在常压下液化属于物理变化 |
| B、液氨燃烧属于置换反应 |
| C、液氨属于混合物 |
| D、X的化学式为N2 |
下列有关化学知识的说法正确的是( )
| A、铜粉在空气中加热后固体质量会增加,因此这个反应不遵守质量守恒定律 | B、凡是含有碳元素的化合物都是有机物 | C、大多数固体物质的溶解度随温度的升高而增大 | D、可燃物只要达到着火点就能燃烧 |
X表示某物质的化学式,X+6O2
6CO2+6H2O 下列说法正确的是( )
| 一定条件 |
| A、X的组成中一定含碳、氢两种元素,可能含氧元素 |
| B、X是氧化物 |
| C、X中碳、氢两种元素的质量比为6:1 |
| D、在上述变化中氧元素从化合态变为游离态 |
工人师傅进行金属切割或金属焊接时使用的氧炔焰,就是乙炔在氧气中燃烧产生的火焰.乙炔(化学式用R表示)在氧气中充分燃烧的化学方程式为:2R+5O2
4CO2+2H2O,则乙炔的化学式为( )
| ||
| A、C2H2 |
| B、C2H4 |
| C、C2H6 |
| D、C2H6O |
在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.下列关于此反应的认识,正确的是( )
| 物质 | X | Y | Z | W |
| 反应前质量/g | 20 | m | 16 | 14 |
| 反应后质量/g | 4 | 6 | 60 | 50 |
| A、若W为水,则X或Y必定为酸或碱 |
| B、参加反应的X与Y的质量比为1:4 |
| C、若X为化合物,Y为单质,则该反应一定为置换反应 |
| D、m的数值为64 |