题目内容
在一个密闭容器中放入X、Y、Z、W四种物质,在一定条件下发生化学反应,一段时间后,测得有关数据如下表.下列关于此反应的认识,正确的是( )
| 物质 | X | Y | Z | W |
| 反应前质量/g | 20 | m | 16 | 14 |
| 反应后质量/g | 4 | 6 | 60 | 50 |
| A、若W为水,则X或Y必定为酸或碱 |
| B、参加反应的X与Y的质量比为1:4 |
| C、若X为化合物,Y为单质,则该反应一定为置换反应 |
| D、m的数值为64 |
练习册系列答案
相关题目
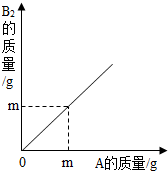 在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,现将8gA和5gB2充分反应,则生成AB2的质量是( )
在化学反应A+B2=AB2中,A与B2反应的质量关系如图所示,现将8gA和5gB2充分反应,则生成AB2的质量是( )| A、10g | B、13g | C、16g | D、18g |
X、Y、M、R四种物质之间存在如下反应:X+Y→M+R,下列说法正确的是( )
| A、10g X与l0g Y充分反应后生成M与R的质量之和一定为20g | B、若Y是氧气,M、R分别是二氧化碳和水,则X中一定 有碳、氢、氧三种元素 | C、X、M是单质,Y、R是化合物,则该反应一定是置换反应 | D、若M、R分别是盐和水,则该反应一定是复分解反应 |
电解氯化钠的水溶液不可能得到的物质是( )
| A、NaNO3 | B、H2 | C、Cl2 | D、NaOH |
守恒思想在以下的化学计算中的应用正确的是( )
| A、14g碳与32g氧气反应,由质量守恒推出生成的二氧化碳的质量为46g | B、蜡烛燃烧生成二氧化碳和水,由元素守恒推出蜡烛由碳、氢、氧元素组成 | C、50 mL98%的硫酸用50 mL水稀释,由溶质守恒推出稀硫酸的溶质质量分数为49% | D、电解水生成H2、O2分子数比为2:l,由原子守恒推出水中H、O原子数比为2:1 |
人们常用金属器皿来盛水,也常用铁、铝或铜制的水壶来烧水,说明这几种金属与热水是不反应的,但金属钠却能与水发生以下反应:2Na+2H2O=2R+H2↑,而R是( )
| A、Na | B、Na2O | C、Na2O2 | D、NaOH |
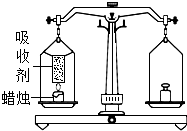 某同学欲用蜡烛燃烧验证质量守恒定律,实验设计如图所示.实验时用吸收剂将产生的水和二氧化碳进行彻底吸收.下列实验现象和分析错误的是( )
某同学欲用蜡烛燃烧验证质量守恒定律,实验设计如图所示.实验时用吸收剂将产生的水和二氧化碳进行彻底吸收.下列实验现象和分析错误的是( )| A、点燃蜡烛后天平指针向右偏转 | B、蜡烛燃烧反应为氧化反应 | C、此实验中生成CO2中的碳元素质量一定等于参加反应蜡烛中碳元素质量 | D、此实验中生成水中的氢元素质量一定等于参加反应蜡烛中氢元素质量 |
某有机物在空气中完全燃烧,测得生成物中二氧化碳、水蒸气、二氧化硫,下列对该有机物的推断正确的是( )
| A、只含有碳、氢元素 | B、一定含有碳、氢、氧元素 | C、一定含有碳、氢、硫元素 | D、一定含有碳、氢、氧、硫元素 |
下列化学方程式,书写完全正确的是( )
A、C+CO2
| ||||
B、CO+Fe2O3
| ||||
| C、Ca(OH)2+HCl=CaCl+H2O | ||||
D、2KMnO4
|
